Решенные упражнения на химические превращения
Вопрос 1
(IFG) Рассмотрим следующую фразу Карла Густава Юнга: «Встреча двух личностей подобна контакту двух химических веществ: если происходит какая-либо реакция, оба претерпевают трансформацию». В этом предложении автор связывает встречу двух людей с процессом химических реакций и превращений. Из перечисленных процессов выберите тот, который нельзя классифицировать как химическую реакцию.
А) Переваривание пищи.
Б) Производство мыла из нефти и едкого натра.
В) сжигание бумаги.
Г) Фотосинтез.
Е) Таяние воды.
Разрешение:
альтернатива Е.
Плавление воды не является химической реакцией, потому что вещество (вода) не изменяет своего химического состава. При таянии лед просто тает, то есть вода переходит из твердого состояния в жидкое, не меняя своего химического состава.
вопрос 2
(UFT) В нашей повседневной жизни мы живем с несколькими процессами, которые называются физическими явлениями и химическими явлениями. Физические явления — это явления, при которых фазовые изменения вещества происходят без изменения его химического состава. Химические явления – это те, которые происходят с изменением химического состава веществ. Что из перечисленного относится только к химическим явлениям?
А) Образование ржавчины, гниение плодов, горение стальной ваты, фотосинтез растениями.
Б) Горение пороха, испарение воды, сгорание бензина, образование льда.
В) Сушка белья на бельевой веревке, пищевой обмен в нашем организме, центрифугирование крови.
Г) Сжигание этанола, перегонка нефти, взрыв фейерверков, плавление поваренной соли.
Д) Образование инея, сушка одежды, образование облаков, таяние льда.
Разрешение:
Альтернатива А.
Только в первом варианте все процессы можно охарактеризовать как химические превращения. В варианте Б испарение воды и образование льда являются физическими явлениями; в альтернативе С сушка одежды на бельевой веревке и центрифугирование крови являются физическими явлениями; в варианте D дистилляция нефти и плавление поваренной соли являются физическими явлениями; а в альтернативе E ни один из процессов не формирует химическое явление.
Стефано Араужо Новаис
Учитель химии
Родственные связи между металлами и неметаллами
Кислород является типичным представителем неметаллов. Он является достаточно сильным окислителем, перед которым может устоять только фтор. Получение основных оксидов происходит путём взаимодействия кислорода и металлов. Однако не все металлы охотно с ним реагируют. Щелочные реагируют бурно, именно поэтому их хранение осуществляется под слоем керосина. Необходимо заметить, что щелочные металлы не образуют оксиды во время взаимодействия с О2. Их чрезвычайная активность позволяет получать только для их характерные продукты, это будут пероксиды и надпероксиды (за исключением лития, продукт Li2O).
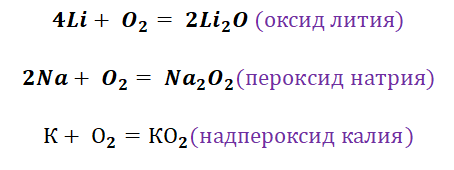
А вот, чтобы менее активные металлы – железо или медь прореагировали, необходимо нагревание.

Получение кислотных оксидов происходит аналогично взаимодействием неметаллов с О2.
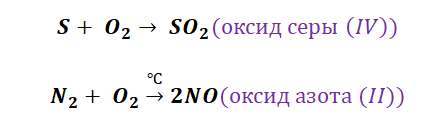
Металлы и неметаллы в химии рассматриваются как противоположности, которые, как заряды (положительные и отрицательные) имеют свойства притягиваться. Рассмотрим на примере металла кальций и неметалла углерод.
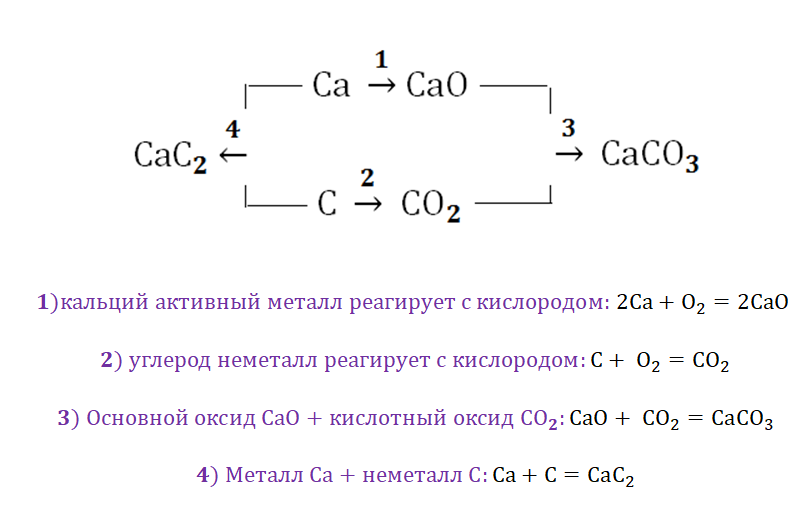
Соль СаСО3 имеет истоки от простых веществ Са и С, промежуточным звеном являются оксиды этих веществ, для которых свойственно реагировать между собой.
Вспомним с Вами один с основных постулатов химии, а именно, закон постоянства состава вещества.
Представим, что мы с Вами химики-первооткрыватели и нам предстоит сложная задача получить азотную кислоту, которая имеет важную роль в химической промышленности. Получение кислот возможно несколькими способами. Обращаясь к таблице 1, делаем вывод, что нам доступно несколько способов, а именно.
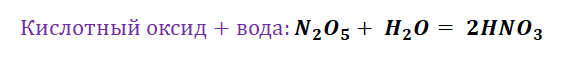
Взаимодействие кислот с солями приведёт нас к желаемому результату, однако не забывайте, что в продукте должны увидеть газ, осадок либо окрашивание.
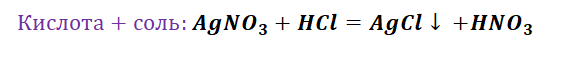
Способы получения средних солей доказательно показывают связь между веществами. Снова выручалочкой нам послужит таблица 1. Наша задача получить вещество, без которого, полагаем, Вы не представляете своё существование, это соль NaCl. Используя данные, видим, что доступно для её получения 4 способа (Вы ищете, где продуктом является соль и применяете данные на свой пример).
Рассмотрим подробно каждый с них.
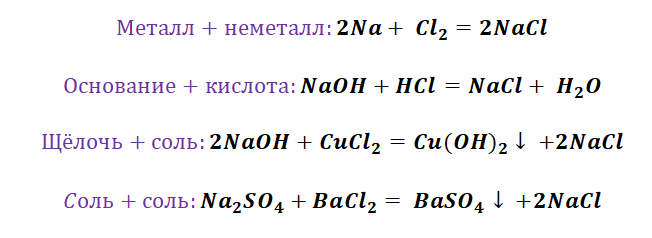
Способы получения солей отличаются, причиной этому является то, какую именно соль мы хотим получить, кислородсодержащей,сильной или слабой кислоты. К примеру, получение Na2SO4 будет отличаться от предыдущего примера с NaCl. Количество способов будет больше, так как это соль кислородсодержащей кислоты.
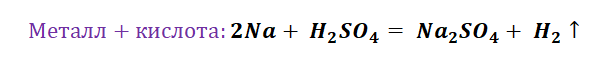
Здесь следуют отметить особенность щелочных, а также щелочно-земельных металлов, для которых свойственно взаимодействие с водой. По сути, идёт два параллельных процесса.
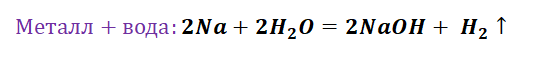
Полученная щёлочь реагирует с кислотой.
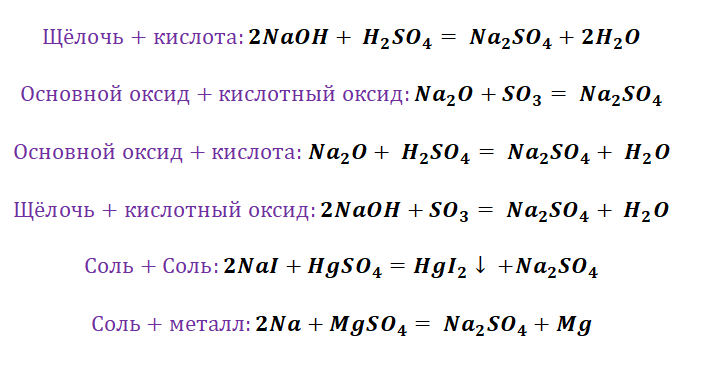
Способы получения солей аммония несколько отличаются, от солей металлов, тем, что аммиак непосредственно реагирует с кислотами (смотри урок химическая связь) с образованием донорно-акцепторных связей.
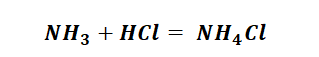
Гидроксид аммония имеет способность взаимодействовать с кислотами, с образованием необходимого продукта, не иначе как солей аммония.
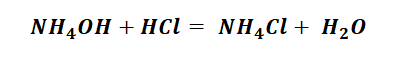
Наверняка некоторые из Вас пугал вид заданий, который был цепочек уравнений. Обобщая всё выше сказанное, рассмотрим несколько примеров.
![]()
Чтобы справится с данной задачей, проанализируем условие. Первое, что необходимо выделить – это количество уравнений (смотрим по стрелочкам, их 5). Второе определим исходное вещество – цинк, металл средней силы. Чтобы получить с него соль (не забываем о таблице 1), можно использовать 3 способа:
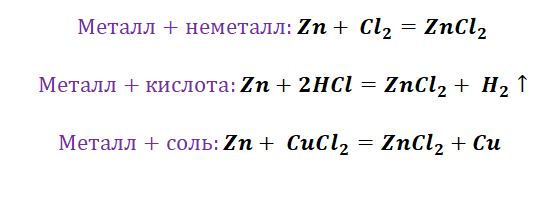
Выбор за Вами, одного из трёх уравнений. Переходим к следующей части цепочки ZnCl2 → Zn(OH)2. Здесь решением будет один вариант, это прибавление щёлочи.
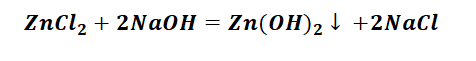
Zn(OH)2 относится к нерастворимым основанием, поэтому при нагревании распадаются.

И наконец, итоговый продукт, металл. Его необходимо выделить из соли. Для этого необходимо взять металл, сила которого будет больше. Если эту информацию забыли, то освежить эти данные сможете с помощью урока Соли и их свойства.
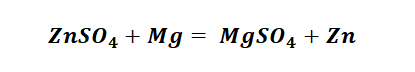
Решение цепочек химических уравнений на первый взгляд кажется не посильной задачей, но если внимательно изучить свойства веществ, то они кажутся не такими уж и сложными.
Повторение. Генетическая связь классов неорганических соединений
Химия – это наука о веществах, их свойствах и превращениях друг в друга.
Рис. 1. Генетическая связь классов неорганических соединений
Все неорганические вещества можно разделить на:
— Простые вещества
— Сложные вещества.
Простые вещества делятся на:
— Металлы
— Неметаллы
Сложные вещества можно разделить на:
— Оксиды
— Основания
— Кислоты
— Соли. См. Рис.1.
Оксиды – это бинарные соединения, состоящее из двух элементов, одним их которых является кислород в степени окисления -2. Рис.2.
Например, оксид кальция: Сu+2О-2,оксид фосфора (V) P2O5., оксид азота (IV) –«лисий хвост»
Рис. 2. Оксиды
Оксиды делятся на:
— Основные
— Кислотные
Основным оксидам соответствуют основания.
Кислотным оксидам соответствуют кислоты.
Соли состоят из катионов металла и анионов кислотного остатка.
Пути генетических связей между веществами
Рис. 3. Пути генетических связей между веществами
Таким образом: из одного класса неорганических соединений можно получить другой класс.
Следовательно, все классы неорганических веществ взаимосвязаны.
Связь классов неорганических соединений часто называют генетической. Рис.3.
Генезис по — гречески означает «происхождение». Т.е. генетическая связь показывает взаимосвязь превращения веществ и их происхождение от единого вещества.
Существует два основных пути генетических связей между веществами. Один из них начинается металлом, другой — неметаллом.
Генетический ряд металла показывает:
Металл → Основной оксид → Соль →Основание → Новая соль.
Генетический ряд неметалла отражает такие превращения:
Неметалл→ Кислотный оксид →Кислота →Соль.
Для любого генетического ряда можно написать уравнения реакций, которые показывают превращения одних веществ в другие.
— Для начала, нужно определить к какому классу неорганических соединений относится каждое вещество генетического ряда.
— Подумать, как из вещества, стоящего до стрелочки, получить вещество стоящие после неё.
Генетический ряд металла
Разложение солей аммония
При разложении солей аммония чаще всего образуется аммиак, исключения составляют соли, в которых анион проявляет окислительные свойства. Например, хлорид, бромид, йодид, сульфиды, карбонаты и фосфаты разлагаются без изменения степеней окисления (без ОВР). Процессы идут при нагревании:
- NH4Cl → NH3↑ + HCl↑ ‒ разложение хлорида аммония
- NH4Br → NH3↑ + HBr↑ ‒ разложение бромида аммония
- NH4I → NH3↑ + HI↑ ‒ разложение йодида аммония
- (NH4)2S → 2NH3↑ + H2S↑ ‒ разложение сульфида аммония
- NH4HS → NH3↑ + H2S↑ ‒ разложение гидросульфида аммония
- (NH4)3PO4 → 3NH3↑ + H3PO4 ‒ разложение фосфата аммония
- (NH4)2HPO4 → 2NH3↑ + H3PO4 ‒ разложение гидрофосфата аммония
- NH4H2PO4 → NH3↑ + H3PO4 ‒ разложение дигидрофосфата аммония
- (NH4)2CO3 → 2NH3↑ + CO2↑ + H2O↑ ‒ разложение карбоната аммония
- NH4HCO3 → NH3↑ + CO2↑ + H2O↑ ‒ разложение гидрокарбоната аммония
Разложение солей аммония с изменением степени окисления:
Разложение нитрита и нитрата аммония легко запомнить вместе, отнимите от этих солей всю воду и получите нужный продукт:
- NH4NO3 → 2H2O + N2O ‒ разложение нитрата аммония
- NH4NO2 → 2H2O + N2 ‒ разложение нитрита аммония
Задание по образцу ФИПИ:
- NH3
- NO
- NH4NO3
- N2
- N2O
Ответ:
Ответить
Азот окисляется до NO
Удобно запоминать вместе и разложение дихромата и перманганата аммония, так как образуются сходные продукты – азот, оксид и соль:
- (NH4)2Cr2O7 → N2↑ + Cr2O3 + 4H2O↑ ‒ разложение дихромата аммония
- 2NH4MnO4 → N2↑ + 2MnO2 + 4H2O↑ ‒ разложение перманганата аммония
Попробуйте решить задание ЕГЭ:
- нитрит аммония
- нитрат аммония
- дихромат аммония
- хлорид аммония
- N2 + Cr2O3 + H2O
- NH3 + Cl2 + H2
- N2 + H2O
- NO2 + Cr2O3 + H2O
- NH3 + HCl
- N2O + H2O
Ответ:
| А | Б | В | Г |
|---|---|---|---|
Ответить
ОСНОВНЫЕ РАЗНОВИДНОСТИ ЦЕПОЧЕК ПРЕВРАЩЕНИЙ
Можно выделить несколько основных разновидностей подобных задач:
1. Цепочки превращений, в которых известны все вещества
Предлагаются формулы конкретных химических веществ. Формулы дают представление о том, к какому (каким) классу (классам) веществ относятся участники цепочки. Это значительно упрощает ее решение. И это, пожалуй, самый простой вид цепочек превращений.
2. Цепочки с неизвестными веществами
Одно из веществ цепи может быть не известно и зашифровано с помощью какой-либо буквы (латиница или кириллица). В таком случае, над стрелкой указывается вещество, которое необходимо добавить к предыдущему, чтобы получилось зашифрованное вещество. Если этого не делать, то можно предположить несколько вариантов решения.
Очень часто вместо химических формул предлагаются названия соединений. Это очень полезно для отработки знаний их номенклатуры и умений по названию определять принадлежность к определенному классу. Например:
В цепочках данного вида могут быть не известны несколько веществ или даже все, кроме одного, например, исходного.
Многие химические элементы имеют несколько степеней окисления. Подобные задачи направлены на знание окислительно-восстановительных свойств веществ и на отработку умений составлять окислительно-восстановительные реакции.
4. Цепочки превращений с неизвестными промежуточными веществами
В подобных случаях предлагаются только исходное вещество и конечный продукт. Так, в данном примере из пропана напрямую получить этиловый эфир аланина невозможно. Промежуточных стадий получения конечного продукта может быть несколько. Это определяет тот, кто решает данную цепочку превращений. Ясно, что и путей решения может быть несколько.
Почему связь между классами веществ считается генетической
Чтобы разобраться в этом вопросе. Вспомним состав классов веществ, с которыми Вы познакомились на предыдущих занятиях.
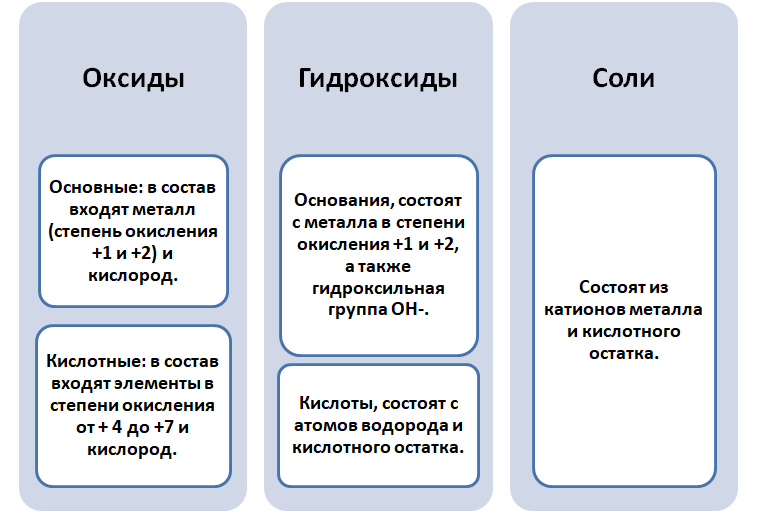
Обратите внимание, что соли содержат в себе частицы как оснований (атомы металла), так и кислот (кислотных остатков). Если соль рассматривать как «венец» превращений, то давайте, попытаемся прийти к истокам
Всё начинается с простого, точнее металла и неметалла, как простых веществ.
Попробуем построить генетический ряд металлов, переходя от одного класса к другому.

Возьмём, к примеру, металлы кальций и медь, подставив их в цепочку уравнений.
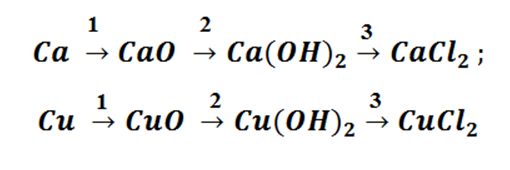
Обратите внимание, что данные металлы отличаются своей реакционной способностью
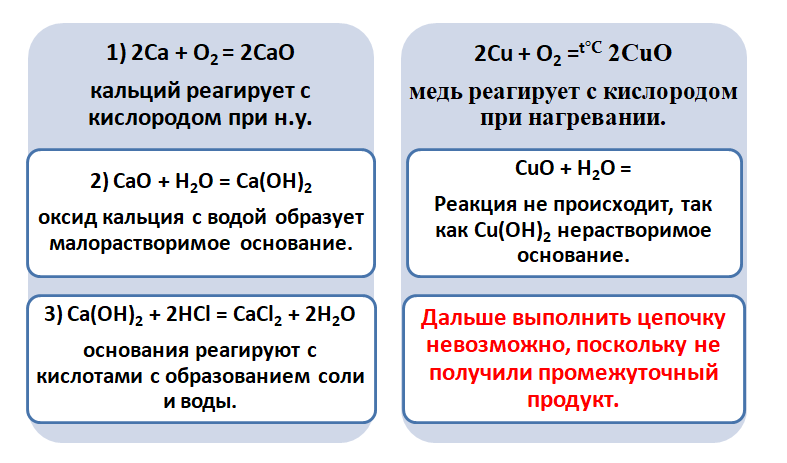
Получается, эта генетическая связь соединений присуща только для активных металлов, оксиды которых, реагируя с водой, дают продукт в виде щёлочи.
Для металлов, которые отличаются малой активностью, переход от вещества, находящегося в простом состоянии, к соли, происходит путём превращений.
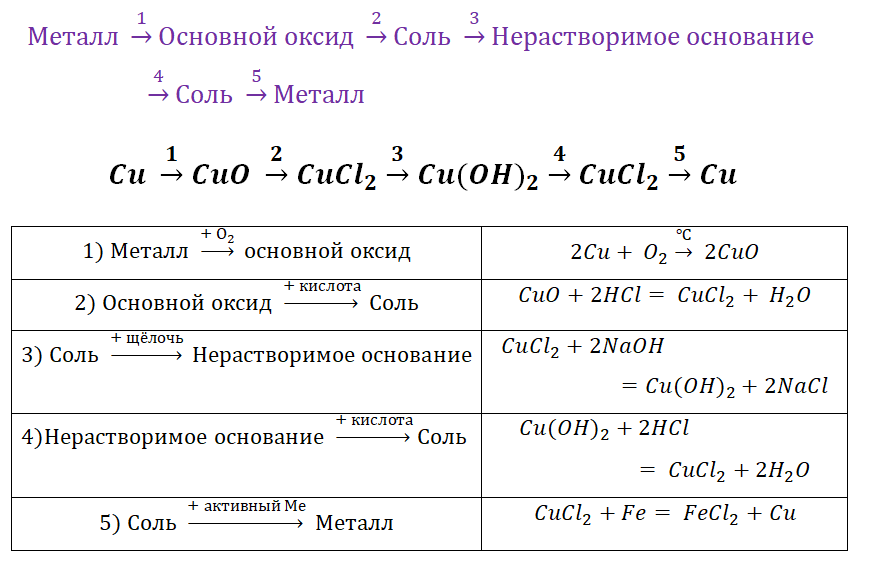
Поскольку основные оксиды реагируют с металлами (более активными, чем металлы, которые входят в состав оксида), то эту схему можно сократить.
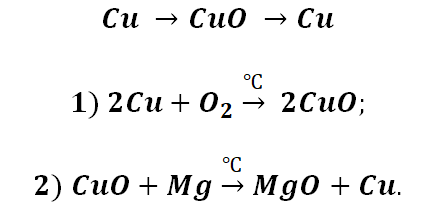
Аналогичным способом можно составить генетический ряд неметаллов, начиная от неметалла заканчивая солью или неметаллом.

Подставим в цепочку уравнений фосфор и кремний.
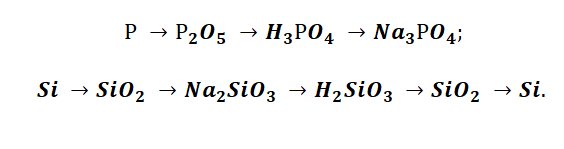
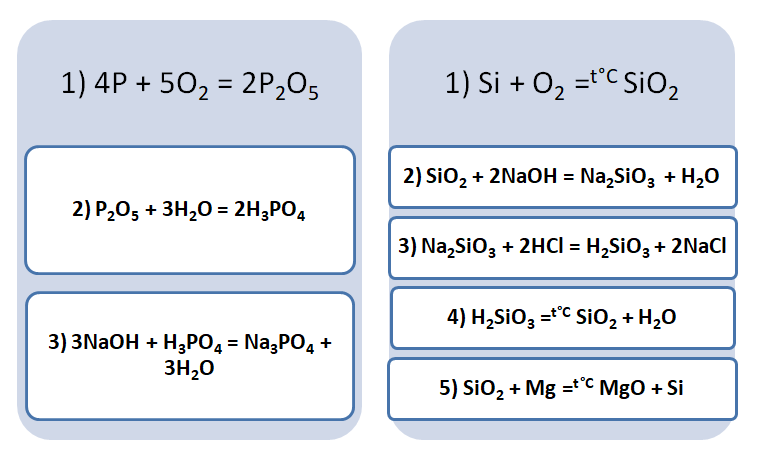
А возможны иные пути решения данных цепочек уравнений. Способы получения кислотных оксидов реализуются путём взаимодействия простых веществ с кислородом. А вот не с каждого оксида можно получить ему соответствующую кислоту, путём прибавления воды. Поскольку кремниевая кислота нерастворима в воде, то необходимо получить сначала соль, а потом уже и кислоту.
В данном решении предлагается добыть соль Na3PO4, взаимодействием основания и кислоты. Однако можно использовать и другие варианты, которые также будут верны.

Если объединить генетические ряды металлов и неметаллов, получим дружную семью неорганических соединений, где каждое вещество связано неразрывной нитью с другими классами. Таблица 1.
Данная таблица отображает, как реагируют между собой вещества и какие продукты возможны, вследствие реакции.
Промоделируем на примере: В вашем распоряжении имеются следующие вещества: оксид серы (VI), гидроксид бария, соляная кислота, карбонат кальция и железо. Ваша задача спрогнозировать, между какими соединениями возможна реакция и, записать, соответствующие уравнения реакций.
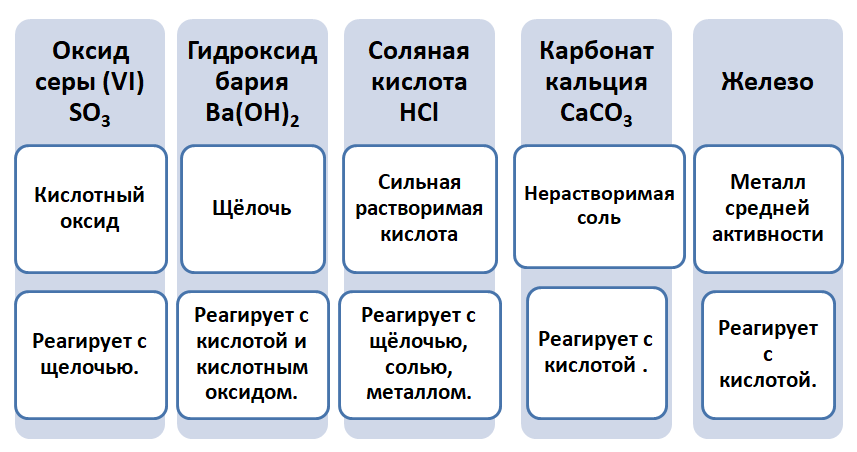
Подтвердив свои прогнозы молекулярно-ионными уравнениями в сокращённом и полном виде.

Готовые работы
КУРСОВЫЕ РАБОТЫ
Курсовой проект — это первая серьезная практическая работа. Именно с написания курсовой начинается подготовка к разработке дипломных проектов. Если студент научиться правильно излагать содержание темы в курсовом проекте и грамотно его оформлять, то в последующем у него не возникнет проблем ни с написанием отчетов, ни с составлением дипломных работ, ни с выполнением других практических заданий. Чтобы оказать помощь студентам в написании этого типа студенческой работы и разъяснить возникающие по ходу ее составления вопросы, собственно говоря, и был создан данный информационный раздел. Стоимость работы от 2 500 тенге
МАГИСТЕРСКИЕ ДИССЕРТАЦИИ
В настоящее время в высших учебных заведениях Казахстана и стран СНГ очень распространена ступень высшего профессионального образования, которая следует после бакалавриата — магистратура. В магистратуре обучаются с целью получения диплома магистра, признаваемого в большинстве стран мира больше, чем диплом бакалавра, а также признаётся зарубежными работодателями. Итогом обучения в магистратуре является защита магистерской диссертации. Мы предоставим Вам актуальный аналитический и текстовый материал, в стоимость включены 2 научные статьи и автореферат. Стоимость работы от 35 000 тенге
ОТЧЕТЫ ПО ПРАКТИКЕ
После прохождения любого типа студенческой практики (учебной, производственной, преддипломной) требуется составить отчёт. Этот документ будет подтверждением практической работы студента и основой формирования оценки за практику. Обычно, чтобы составить отчёт по практике, требуется собрать и проанализировать информацию о предприятии, рассмотреть структуру и распорядок работы организации, в которой проходится практика, составить календарный план и описать свою практическую деятельность. Мы поможет написать отчёт о прохождении практики с учетом специфики деятельности конкретного предприятия.
Генетическая связь
– это связь между веществами, которые относятся к разным классам.
Основные признаки генетических рядов:
1. Все вещества одного ряда должны быть образованы одним химическим элементом.
2. Вещества, образованные одним и тем же элементом, должны принадлежать к различным классам химических веществ.
3. Вещества, образующие генетический ряд элемента, должны быть связаны между собой взаимопревращениями.
Таким образом, генетическим
называют ряд веществ, которые представляют разные классы неорганических соединений, являются соединениями одного и того же химического элемента, связаны взаимопревращениями и отражают общность происхождения этих веществ.
Для металлов выделяют три ряда генетически связанных веществ, для неметаллов — один ряд.
Генетические ряды
Простые вещества – металлы и неметаллы – образуют цепочки превращений, отражающие генетическую связь неорганических веществ. Посредством химических реакций присоединения, замещения и разложения образуются новые более простые или сложные соединения.
Каждое звено цепочки связано с предыдущим наличием простого вещества. Различие между двумя типами генетических рядов заключается в реакции с водой: металлы образуют растворимые и нерастворимые основания, неметаллы – кислоты.
Основные цепочки превращений описаны в таблице.
|
Вещество |
Генетический ряд |
Примеры |
|
Металл |
Активный металл → основный оксид → щёлочь → соль |
– 2Са + О2 → 2CaO; – CaO + Н2О → Ca(ОН)2; – Ca(ОН)2 + 2HCl → CaCl2 + 2H2O |
|
Малоактивный металл → основный оксид → соль → нерастворимое основание → основный оксид → металл |
– 2Cu + O2 → 2CuO; – CuO + 2HCl → CuCl2 + H2O; – CuCl2 + 2KOH → Cu(OH)2 + 2KCl; – Cu(OH)2 → CuO + H2O; – CuO + H2 → Cu + H2O |
|
|
Неметалл |
→ кислотный оксид → растворимая (сильная) кислота → соль |
– 4P + 5O2 → 2P2O5; – P2O5 + 3H2O → 2H3PO4; – H3PO4 + 3NaOH → Na3PO4 + 3H2O |
|
→ кислотный оксид → соль → нерастворимая (слабая) кислота → кислотный оксид → неметалл |
– Si + O2 → SiO2; – SiO2 + 2NaOH → Na2SiO3 + H2O; – Na2SiO3 + 2HCl → H2SiO3 + 2NaCl; – H2SiO3 → SiO2 + H2O; – SiO2 + 2Zn → 2ZnO + Si |
Рис. 3. Схема генетической связи между классами.
С помощью цепочки превращения можно получить средние (нормальные) или кислые соли. Комплексные соли могут включать несколько атомов металлов и неметаллов.
Что мы узнали?
Генетическая связь показывает взаимосвязь между классами неорганических веществ. Она характеризуется генетическим рядом – чередой превращений простых веществ. К простым веществам относятся металлы и неметаллы. Металлы образуют растворимые и нерастворимые основания в зависимости от активности. Неметаллы превращаются в сильные или слабые кислоты. Новые сложные вещества ряда образуются реакциями присоединения, замещения и разложения.
-
/5
Вопрос 1 из 5
Неорганические вещества
Соединения, не имеющие углеродного скелета, характерного для органических веществ, называются неорганическими или минеральными веществами. Все минеральные соединения классифицируются на две обширные группы:
К простым соединениям относятся:
- металлы (K, Mg, Ca);
- неметаллы (O2, S, P);
- инертные газы (Kr, Xe, Rn).
Сложные вещества имеют более разветвлённую классификацию, приведённую в таблице.
Класс
Подкласс
Примеры
Рис. 2. Классификация сложных веществ.
Амфотерные металлы образуют соответствующие оксиды и гидроксиды. Амфотерные соединения проявляют свойства кислот и оснований.
Алгоритм решения «цепочек превращений» веществ. Инструкция для учащихся 8 класса
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах. Алгоритм решения «цепочек превращения» по химии
Алгоритм решения «цепочек превращения» по химии
В химии есть задания со схемами превращений одних веществ в другие, которые характеризуют генетическую связь между основными классами органических и неорганических соединений.
Схему превращения одних веществ в другие называют «цепочкой превращений » .
Для выполнения этих заданий необходимо знать основные классы соединений, их номенклатуру, химические свойства, механизм осуществления реакций.
Алгоритм решения «цепочки превращений»
1 шаг. Перепишите цепочку, которую необходимо решить
2 шаг. Пронумеруйте количество реакций для удобства решения
Таким образом, мы видим, что нам надо составить 3 уравнения реакции
3 шаг. Запишем 1 уравнение реакции – из кальция (С a ) надо получить оксид кальция ( CaO ). Вспомним, что данное превращение происходит, когда металлы окисляются на воздухе, вступая в реакцию с кислородом. Записываем эту реакцию
Внимание! Не забывайте уравнивать реакции!
2 С a + O 2 2Ca +2 O -2
4 шаг. Осуществляем второе превращение. Из оксида кальция ( CaO ) нужно получить гидроксид кальция ( Ca ( OH ) 2 ). Это уравнение возможно при взаимодействии оксида с водой. (Такая реакция возможна, если в итоге получается щелочь – растворимое в воде основание). Записываем уравнение и уравниваем его.
2) 2 Ca +2 O -2 + H 2 O → Ca 2+ ( OH ) 2 —
5 шаг . Осуществляем 3 превращение. Из гидроксида кальция ( Ca ( OH ) 2 ) необходимо получить соль – фосфат кальция ( Ca 3 ( PO 4 ) 2 ). Вспоминаем, что при взаимодействии основания и кислоты получается соль и вода. Значит, для этой реакции подойдет фосфорная кислота – H 3 PO 4 , так как именно она дает соли – фосфаты. Записываем уравнение реакции и уравниваем его.
Курс повышения квалификации
Сейчас обучается 939 человек из 80 регионов
Курс повышения квалификации
- Курс добавлен 31.01.2022
- Сейчас обучается 23 человека из 14 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
Сейчас обучается 40 человек из 24 регионов
Ищем педагогов в команду «Инфоурок»
Видео:Задание 21 – решаем на максимум | Химия ОГЭ 2023Скачать

Классификация
Все неорганические соединения делятся на две обширные группы:
- простые, состоящие из одинаковых атомов;
- сложные, состоящие из атомов разных соединений.
Простые вещества классифицируются на металлы и неметаллы.
Рис. 1. Классификация неорганических веществ.
К металлам относятся элементы I-II группы и побочные подгруппы III-VIII групп таблицы Менделеева. Это твёрдые вещества (исключение – ртуть), имеющие блеск и обладающие тепло- и электропроводностью. Примеры: натрий, кальций, железо, хром.
К неметаллам относятся газообразные, жидкие, твёрдые вещества, вступающие в реакции с металлами и между собой. Примеры: хлор, водород, сера, йод, бром.
Сложные вещества разделяются на четыре группы:
- основные и кислотные оксиды;
- основания;
- кислоты;
- соли.
Сложные вещества состоят из простых, которые могут отделяться от одного соединения и образовывать новые соединения.
 Рис. 2. Примеры сложных веществ.
Рис. 2. Примеры сложных веществ.
Наиболее сложными неорганическими соединениями являются соли, которые могут включать несколько атомов металлов и неметаллов.
ЦЕПОЧКИ ПРЕВРАЩЕНИЙ: ОСНОВНОЙ АЛГОРИТМ РЕШЕНИЯ
На конкретном примере рассмотрим основной алгоритм решения:
1) записываем цепочку;
2) под формулами веществ подписываем их названия;
3) над стрелками ставим номера реакций;
4) решаем цепочку, записывая каждую реакцию под своим номером;
5) если требуется, над стрелками в реакциях указываем условия протекания реакций.
Цепочки превращений направлены на закрепление и углубление знаний химических свойств веществ и способов их получения. Они помогают развивать логическое мышление, память, умение выявлять закономерности. Часто требуют не стандартного подхода к решению.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.

Разложение нитратов
При установлении продуктов термического разложения нитратов удобно пользоваться рядом активности металлов, однако к нему следует добавить некоторые уточнения: литий и магний, обычно относятся к активным металлам, но разложение нитратов этих двух металлов происходит как у металлов средней активности. Медь относится к неактивным металлам, но разложение нитрата меди II идёт как разложение нитрата металла средней активности. Данные реакции являются весьма популярными в химии. На ЕГЭ задачи по разложению нитратов встречаются в заданиях линии 7 и 31.
Уравнения разложения нитратов активных металлов (кроме лития и магния):
- 2KNO3 → 2KNO2 + O2↑ ‒ разложение нитрата калия
- 2NaNO3 → 2NaNO2 + O2↑ ‒ разложение нитрата натрия
- 2CsNO3 → 2CsNO2 + O2↑ ‒ разложение нитрата цезия
- 2RbNO3 → 2RbNO2 + O2↑ ‒ разложение нитрата рубидия
- Ca(NO3)2 → Ca(NO2)2 + O2↑ ‒ разложение нитрата кальция
- Ba(NO3)2 → Ba(NO2)2 + O2↑ ‒ разложение нитрата бария
- Sr(NO3)2 → Sr(NO2)2 + O2↑ ‒ разложение нитрата стронция
Уравнения разложения нитратов металлов средней активности, нитрата лития и нитрата меди II:
- 4LiNO3 → 2Li2O + 4NO2↑ + O2↑ ‒ разложение нитрата лития
- 2Mg(NO3)2 → 2MgO + 4NO2↑ + O2↑ ‒ разложение нитрата магния
- 2Zn(NO3)2 → 2ZnO + 4NO2↑ + O2↑ ‒ разложение нитрата цинка
- 2Cu(NO3)2 → 2CuO + 4NO2↑ + O2↑ ‒ разложение нитрата меди II
- 4Al(NO3)3 → 2Al2O3 + 12NO2↑ + 3O2↑ ‒ разложение нитрата алюминия
- 4Fe(NO3)3 → 2Fe2O3 + 12NO2↑ + 3O2↑ ‒ разложение нитрата железа III
- 4Cr(NO3)3 → 2Cr2O3 + 12NO2↑ + 3O2↑ ‒ разложение нитрата хрома III
Во всех приведенных реакциях степень окисления металла не изменяется. Это характерно для нитратов, содержащих металл в высшей или наиболее устойчивой степени окисления. Если же нитрат образован переходным металлом в низшей степени окисления, то при разложении этого нитрата происходит окисление еще и металла.






























