Электронная оболочка атома
Число электронов в оболочке атома равно числу протонов в ядре, ему соответствует атомный номер элемента в таблице Д. И. Менделеева.
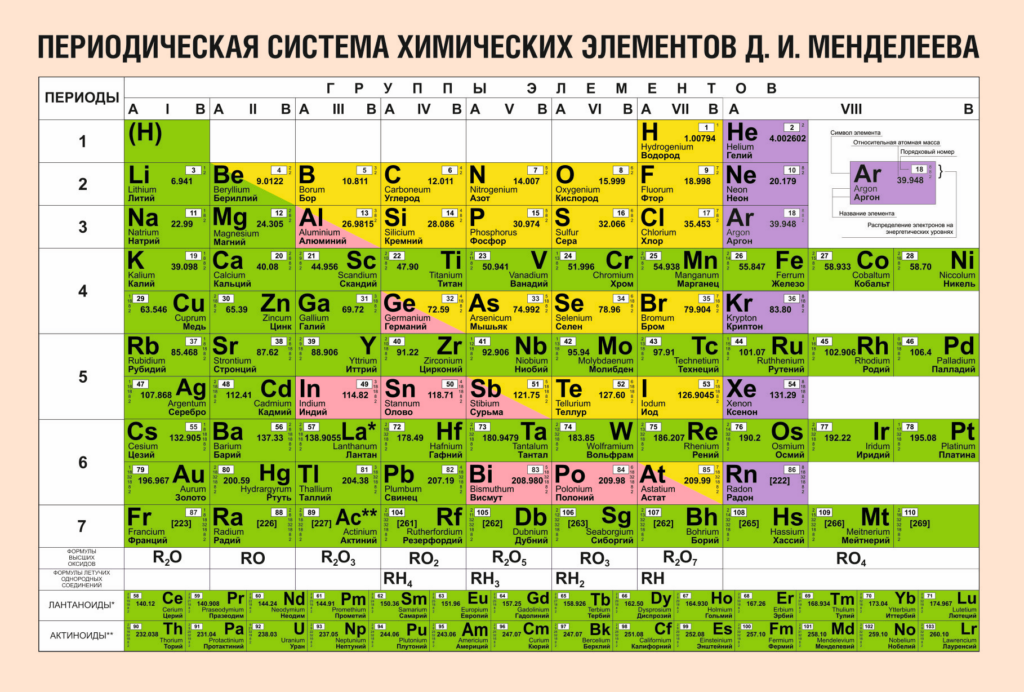
Рисунок 2. Периодическая система химических элементов Д. И. Менделеева
Например, электронная оболочка магния состоит из двенадцати электронов, водорода — из одного, кальция — из двадцати.
Рисунок 3. Атомные номера магния, водорода и кальция в Периодической системе химических элементов Д. И. Менделеева
Возникает вопрос, как движутся электроны вокруг ядра? Есть ли определенный порядок движения или все происходит хаотично? Как выяснилось, движение электронов вокруг ядра происходит в определенном порядке.
В атоме электроны различаются по энергии. По опытным данным исследователи определили, что одни из них притягиваются к атому слабее, а другие — сильнее.
Основной причиной этого является разное удаление электронов от ядра атома. Чем ближе электрон к ядру, тем прочнее их связь, и тем сложнее «вырвать» его из электронной оболочки. Соответственно, чем дальше электрон от ядра, тем легче его «оторвать».
По мере удаления от ядра атома запас энергии электрона ($Е$) увеличивается.
Рисунок 4. Максимальное число электронов на энергетическом уровне
{"questions":,"answer":0}},"hints":},{"content":"Чему равно число электронов в атоме?`choice-7`","widgets":{"choice-7":{"type":"choice","options":,"explanations":,"answer":}},"hints":}]}
Модели
Помимо модели Бора/Резерфорда были и другие, например, модель Томпсона, полагавшего, что атом является положительно заряженным телом, внутри которого располагаются электроны. Эту модель опроверг Резерфорд.
Также стоит отметить планетарную модель атома Нагаоки, предполагавшего, что строение атома подобно планете Сатурн, у которого вокруг ядра вращаются объединенные в кольца электроны.
Закономерным развитием общепризнанной планетарной модели Бора/Резерфорда стала квантовая модель строения атома, утверждающая, что в ядре атома находятся не имеющие заряда нейтроны, положительно заряженные протоны, а вокруг летают отрицательно заряженные электроны. При этом траектории движения электронов согласно законам квантовой механики наперед не заданы.
Разумеется, все модели строение атомы являются весьма упрощенными вариантами, подлинное строение атома куда более сложное.
Размер атомов в миллионы раз меньше размеров клеток[править]
Атомы не имеют отчётливо выраженной внешней границы, поэтому их размеры часто определяют по расстоянию между ядрами соседних атомов, которые образовали химическую связь. Половина этого расстояния — радиус атома.
Есть и другой вариант определения радиуса атома (см. статью Размер атомов).
В периодической системе элементов размер атома увеличивается при движении сверху вниз по столбцу и уменьшается при движении по строке слева направо. Соответственно, самый маленький атом — это атом гелия, имеющий радиус 32 пм, а самый большой — атом цезия (225 пм). Эти размеры в тысячи раз меньше длины волны видимого света (400—700 нм), поэтому атомы нельзя увидеть в оптический микроскоп. Однако отдельные атомы можно наблюдать (например, на поверхности металлов) с помощью сканирующего туннельного микроскопа. Диаметр ядра атома примерно в 100.000 раз меньше диаметра самого атома.
Радиус зависит от положения атома, его типа, вида химической связи, числа ближайших атомов (координационного числа) и квантово-механического свойства, известного как спин.
Малость атомов демонстрируют следующие примеры. Человеческий волос по толщине в миллион раз больше атома углерода. Толщина человеческого волоса примерно 105 нм, а 10 углеродных атомов, выстроенных в цепочку, по толщине составляют 1 нм. Одна капля воды содержит 2 x 10 21 атомов кислорода и в два раза больше атомов водорода. Если бы яблоко можно было увеличить до размеров Земли, то атомы достигли бы исходных размеров яблока.
Клетка мелкой бактерии имеет объем около 1 мкм³. Даже в такой мелкой клетке содержится несколько миллионов атомов.
Правило Хунда и принцип Паули
Правило Хунда — правило квантовой химии, определяющее порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Другая формулировка: Ниже по энергии лежит тот атомный терм, для которого выполняются два условия.
- Мультиплетность максимальна
- При совпадении мультиплетностей суммарный орбитальный момент L максимален.
Разберём это правило на примере заполнения орбиталей p-подуровня p-элементов второго периода (то есть от бора до неона (в приведённой ниже схеме горизонтальными чёрточками обозначены орбитали, вертикальными стрелками — электроны, причём направление стрелки обозначает ориентацию спина).
При́нцип Па́ули (принцип запрета) — один из фундаментальных принципов квантовой механики, согласно которому два и более тождественных фермиона (частицы с полуцелым спином) не могут одновременно находиться в одном и том же квантовом состоянии.
Правило Хунда и принцип Паули
Строение атома
Сегодня мы будем путешествовать в микромир – мир атома. Даже если превратить нас в песчинку, то по сравнению с размером ядра атомов химических элементов, мы будем гигантами.
Атом нельзя увидеть, невозможно потрогать, он на столько мал, что существует только в нашем воображении. До XIX века учёные оперировали только одной характеристикой атома – это его масса. Наука не оперировала понятиями, что ядро атома содержит более мелкие частицы. Почему элементы отличаются массой. Атом долгое время считали «неделимым». Но отличия в массе подвигли искать причину в строении.
Как описать строение, то чего невозможно увидеть, а можно только представить. Ведь современные электронные микроскопы появились только в XX веке.
Атом – как мельчайшая частица, известна ещё с древних времён. Древнегреческий философ Демокрит считал, что свойства веществ определяются определённым типом атома. Даже тонкая материя, душа, по его мнению, состоит из атомов. Так тела бывают в разных агрегатных состояниях, поэтому атомы металлов будут с зубцами, жидкости будут обладать гладкими, это будет причиной их текучести.
Долгое время атом считали неделимым. Заглянув в словарь синонимов, можно увидеть пару синонимов для слова атом, неделимый, мельчайшая частица. Теория о неделимости существовала до XIX века, пока экспериментально не подтвердили, что ядро атома состоит из более мелких частиц. Но как они располагаются в атоме, как конфеты драже в кармашке, или по версии Томсона, который сравнивал электроны с изюминками, хаотично разбросанных в кексе. Учёный с Японии Хантаро Нагаока сравнил атом с загадочной планетой Сатурн, которая известна своим кольцом. Саму планету он сравнил с массивным ядром, а роль кольца отдал электронам.
В конце XIX века, начале XX происходит стремительное развитие науки, открываются новые частицы α и β. Позже было установлено, что это ядро атома элемента Не и электроны.
Английский физик Резерфорд сравнил атом с Солнечной системой. Солнце – это очень большая звезда, которая находится в центре. Масса Солнца занимает 99,86 % от массы всей Солнечной системы. Подобно планетам, электроны вращаются вокруг ядра, каждый из них занимает своё положение — орбиталь. Т.е. электроны – это оболочка атома.

В ходе данных исследований было доказано, что атом представляет совокупность заряженных и нейтральных частичек.
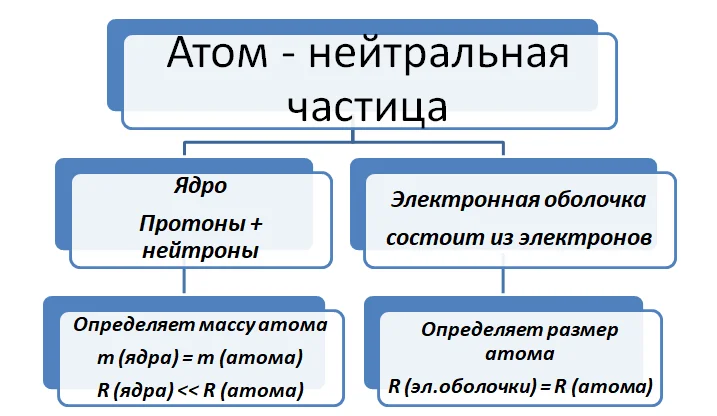
Анализируя размеры, важно запомнить, что радиус ядра атома, будет всегда значительно меньше радиуса всего атома. Этот факт объясняется тем, что частицы составляющие ядро более компактно упакованы, чем электроны
Атом — наименьшая частица химического элемента[править]
Атом гелия
А́том (др.-греч. ἄτομος — неделимый) — наименьшая частица химического элемента, являющаяся носителем его свойств. Атом состоит из атомного ядра и окружающего его электронного облака. Ядро атома состоит из положительно заряженных протонов и электрически нейтральных нейтронов, а окружающее его облако состоит из отрицательно заряженных электронов.
Поскольку число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. Атом, который отдал или приобрел электроны, обладает некоторым положительным или отрицательным зарядом и называется ионом (ион может представлять собой и группу атомов — часть молекулы).
Атомы классифицируются по числу протонов и нейтронов в ядре: число протонов определяет принадлежность атома некоторому химическому элементу. Число нейтронов у атомов одного химического элемента может различаться, атомы с одинаковым числом протонов, но разным числом нейтронов называют изотопами данного элемента.
Атомы, связанные межатомными связями, образуют молекулы.
Модели атомов
В разные эпохи предлагались различные модели атомов, наиболее известная из которых — планетарная модель атома Бора-Резерфорда. В 1911 году Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а следовательно, терять энергию. Расчеты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает («модель атома Бора-Резерфорда»). Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
Современные представления об атоме
Сегодня общепринятой является модель атома, являющаяся развитием планетарной модели. Считается, что ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами.
Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома).
Химические свойства атомов определяются конфигурацией электронной оболочки и описываются c помощью квантовой механикой. Положение атома в таблице Менделеева определяется числом протонов, в то время как число нейтронов принципиально на химические свойства не влияет; при этом нейтронов в ядре, как правило, не меньше, чем протонов (см. атомное ядро). Если атом находится в нейтральном состоянии, то число электронов в нём равно числу протонов. Основная масса атома сосредоточена в ядре, а массовая доля электронов в общей массе атома незначительна (несколько сотых процента массы ядра).
Массу атома принято измерять в атомных единицах массы, равных 1/12 от массы атома стабильного изотопа углерода 12C.
Страницы
- Главная страница
- ОСНОВЫ ОБЩЕЙ ХИМИИ
- 1.1 Важнейшие классы неорганических веществ
- 2.1 Вещества. Атомы
- 2.2 Размеры атомов
- 2.3 Молекулы. Химические формулы
- 2.4 Простые и сложные вещества
- 2.5 Валентность элементов
- 2.6 Моль. Молярная масса
- 2.7 Закон Авогадро
- 2.8 Закон сохранения массы веществ
- 2.9 Вывод химических формул
- 3.1 Строение атома. Химическая связь
- 3.2 Строение атома
- 3.4 Строение электронной оболочки атома
- 3.5 Периодическая система химических элементов
- 3.6 Зависимость свойств элементов
- 3.7 Химическая связь и строение вещества
- 3.8 Гибридизация орбиталей
- 3.9 Донорно-акцепторный механизм образования
- 3.10 Степени окисления элементов
- 4.1 Классификация химических реакций
- 4.2 Тепловые эффекты реакций
- 4.3 Скорость химических реакций
- 4.4 Необратимые и обратимые реакции
- 4.5 Общая классификация химических реакций
- НЕОРГАНИЧЕСКАЯ ХИМИЯ
- 5.1 Растворы. Электролитическая диссоциация
- 5.2 Количественная характеристика состава растворов
- 5.3 Электролитическая диссоциация
- 5.4 Диссоциация кислот, оснований и солей
- 5.5 Диссоциация воды
- 5.6 Реакции обмена в водных растворах электролитов
- 5.7 Гидролиз солей
- 6.1 Важнейшие классы неорганических веществ
- 6.2 Кислоты, их свойства и получение
- 6.3 Амфотерные гидроксиды
- 6.4 Соли, их свойства и получение
- 6.5 Генетическая связь между важнейшими классами
- 6.6 Понятие о двойных солях
- 7.1 Металлы и их соединения
- 7.2 Электролиз
- 7.3 Общая характеристика металлов
- 7.4 Металлы главных подгрупп I и II групп
- 7.5 Алюминий
- 7.6 Железо
- 7.7 Хром
- 7.8 Важнейшие соединения марганца и меди
- 8.1 Неметаллы и их неорганические соединения
- 8.2 Водород, его получение
- 8.3 Галогены. Хлор
- 8.4 Халькогены. Кислород
- 8.5 Сера и ее важнейшие соединения
- 8.6 Азот. Аммиак. Соли аммония
- 8.7 Оксиды азота. Азотная кислота
- 8.8 Фосфор и его соединения
- 8.9 Углерод и его важнейшие соединения
- 8.10 Кремний и его важнейшие соединения
- ОРГАНИЧЕСКАЯ ХИМИЯ
- 9.1 Основные положения органической химии. Углеводороды
- 9.2 Электронные эффекты заместителей в органических соединениях
- 9.3 Предельные углеводороды (алканы)
- 9.3.1 Насыщенные УВ. Метан
- 9.4 Понятие о циклоалканах
- 9.5 Непредельные углеводороды
- 9.6 Диеновые углеводороды (алкадиены)
- 9.7 Алкины
- 9.8 Ароматические углеводороды
- 9.9 Природные источники углеводородов
- 10.1 Кислородсодержащие органические соединения
- 10.2 Фенолы
- 10.3 Альдегиды
- 10.4 Карбоновые кислоты
- 10.5 Сложные эфиры. Жиры
- 10.6 Понятие о поверхностно-активных веществах
- 10.7 Углеводы
- 11.1 Амины. Аминокислоты
- 11.2 Белки
- 11.3 Понятие о гетероциклических соединениях
- 11.4 Нуклеиновые кислоты
- 12.1 Высокомолекулярные соединения
- 12.2 Синтетические волокна
Ядро атома
Орешки фундука явно вы видели. В середине ореха находится большое ядро, занимающее почти всю массу ореха, оставляя малое пространство между скорлупой.
Ядро атома элемента имеет в составе протоны и нейтроны, которые принято называть нуклонами.
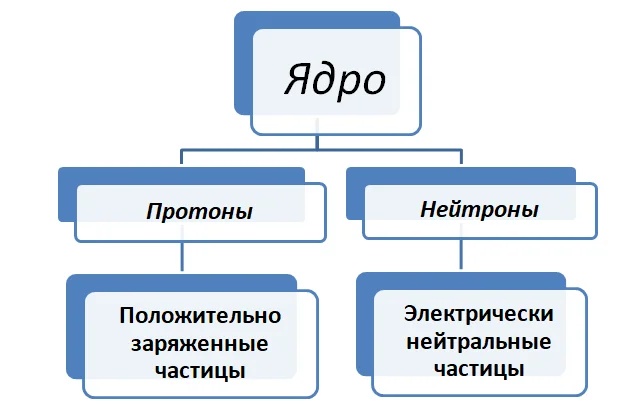
Данные частицы не относятся к элементарным, научно доказано, что они состоят с кварков (в словарь). Нейтроны в ядре атома не несут никакого заряда, они нейтральны. Протоны в ядре атома определяют его заряд.
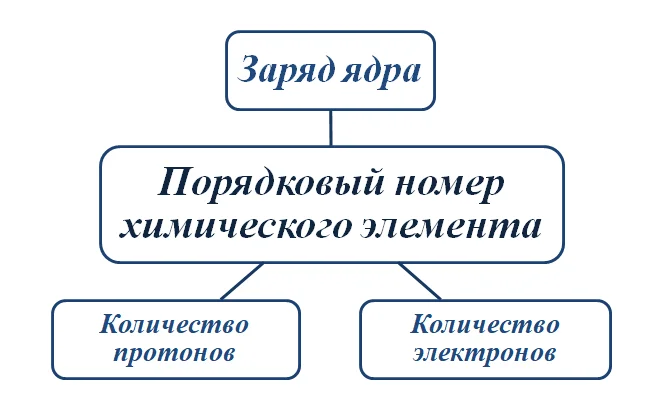
Сумма протонов и нейтронов составляет массовое число ядра атома (нуклонное).
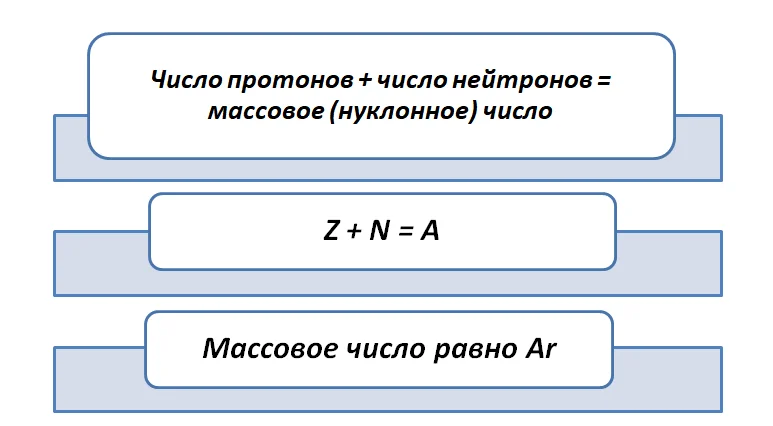
Вы наверняка замечали, что значение Ar в ПСХЭ имеет вид не целого числа, с чем это связано? Причина кроется в том, что химические элементы существуют в виде изотопов.
Чтобы понять суть этого понятия, давайте вспомним, чем особенный каждый элемент? Заряд ядра атома постоянен, другими словами, неизменимое количество протонов. Значит, это будет разновидность элементов, которые будут отличаться нуклонным числом, и как следствие, количеством нейтронов.
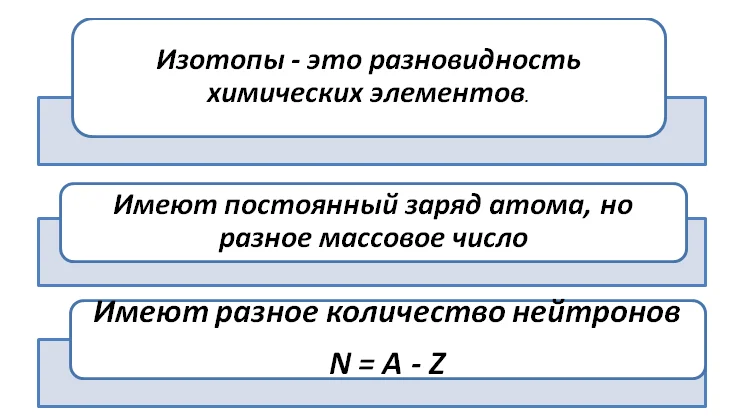
Именно по причине существования изотопов, Ar не имеет целого числового значения. Например, количество изотопов хлора – 2.
Масса изотопов и их процентное содержание составляют относительную массу элемента.
Возможно, вы ранее замечали, что в ПСХЭ есть пара элементов, которые нарушают порядок размещения по увеличению относительной атомной массы. Это пары K – Ar, Co – Ni, Te – I.

Некоторые изотопы отличаются особенной способностью самовольно превращаться в другие элементы – это явление носит название радиоактивность, а сами элементы – радиоактивные. Таким образом, они делятся на стабильные и радиоактивные изотопы.
Изотопы элементов после Висмута в ПСХЭ, начиная с 84, будут относиться к радиоактивным элементам.
В ходе распада радиоактивного изотопа образуются новые элементы, также могут выделяться частицы α (ядра атома ), β – это поток электронов ( , γ – это поток электромагнитных нейтральных частиц – фотонов.
Современные представления о строении атома
Элемент ЕГЭ: 1.1 Современные представления о строении атома. 1.1.1 Строение электронных оболочек атомов элементов первых четырех периодов: s-, р- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояние атомов.
Содержание (быстрый переход):
Современные представления о строении атома
Атом – химически неделимая электронейтральная частица, которая состоит из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов.
Атомы не имеют заряда (нейтральны). Если атом присоединяет один или несколько электронов, он приобретает отрицательный заряд и превращается в анион. Если атом теряет один или несколько электронов, он приобретает положительный заряд и превращается в катион. Заряд иона указывают арабской цифрой и знаком после символа атома.
Состав ядра: А = Z + N, где А — массовое число; Z — протонное число (число протонов); N — число нейтронов.
Элементарные частицы
| Название | Обозначение | Масса | Заряд |
| Электрон |
ē |
≈ 0 | -1 |
| Протон |
р |
1 | +1 |
| Нейтрон |
n |
1 |
Порядковый номер элемента в периодической системе:
- Заряд ядра атома
- Число протонов в ядре атома
- Число электронов в атоме
Нуклиды – разновидности атомов с фиксированным массовым числом А, числом протонов Z и нейтронов N в ядре.
Основные положения квантовой теории строения атома:
- Дискретность энергии электрона
- Двойственная (корпускулярно-волновая) природа электрона
- Невозможность определения траектории электрона (принцип неопределенности)
Относительная атомная масса элемента (Ar)
Физическая величина, показывающая, во сколько раз средняя масса атомов данного элемента больше 1/12 части массы изотопа углерода 12С.
Порядок заполнения орбиталей в основном состоянии
1) Принцип наименьшей энергии. Электроны занимают в первую очередь орбитали, имеющие наименьшую энергию.
2) Принцип Паули. На каждой орбитали могут находиться не более двух электронов, причём спины их противоположны.
3) Правило Хунда. Орбитали заполняются электронами так, чтобы их суммарный спин был максимальным.
Спин электрона — свойство электрона, характеризующее его способность взаимодействовать с магнитным полем. Может принимать два значения (положительное и отрицательное).
Последовательность заполнения орбиталей электронами в основном состоянии:
Энергетические уровни и подуровни
Элементы, у которых идет заполнение s-подуровня, называют s-элементами.
Элементы, у которых заполняется р-подуровень, называют р-элементами.
Элементы, у которых заполняется d-подуровень, называют d-элементами.Элементы, у которых заполняется f-подуровень, называют f-элементами.
Электроны, относящиеся к последнему энергетическому уровню, называют внешними (валентными) электронами.
Строение электронных оболочек атомов первых четырёх периодов
Распределение электронов по орбиталям атома называют электронной конфигурацией атома, или электронной формулой.
Строение элементов четвёртого периода
Электронные конфигурации d5 и d10 обладают повышенной устойчивостью, поэтому в атомах хрома и меди наблюдается «перескок» электрона с 4s-подуровня на 3d-подуровень («провал электрона»).
Основное и возбуждённое состояние атомов
Наиболее устойчивое состояние атома, в котором энергия его электронной оболочки минимальна, называется основным состоянием атома. Любые другие состояния атома называют возбужденными состояниями.
Для возможности перехода атома в возбуждённое состояние необходимо выполнение одновременно двух условий:
- наличие спаренных электронов;
- наличие вакантных орбиталей.
Таблица «Современные представления о строении атома. Кратко»
(с) В учебных целях использованы цитаты из пособий: «Химия / Н. Э. Варавва, О. В. Мешкова. — Москва, Эксмо (ЕГЭ. Экспресс-подготовка)» и «Химия : Новый полный справочник для подготовки к ЕГЭ / Е.В. Савинкина. — Москва, Издательство АСТ».
Вы смотрели Справочник по химии «Современные представления о строении атома». Выберите дальнейшее действие:
- Перейти к Списку конспектов по химии (по классам)
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
- Конспект урока в 11 классе «Основные сведения о строении атома»
Наглядная запись
Теперь возьмём для примера какой-нибудь химический элемент. Например, калий. В таблице Менделеева он имеет запись K и его можно найти под номером 19. Значит, у него имеется 19 электронов, которые нужно расфасовать по орбиталям в указанном порядке. Делаем это.

Сначала идёт уровень 1s. Подуровень s может содержать только 2 электрона. Число электронов записывается в виде маленького индекса над буквой. В данном случае это будет 1s2.
Следом по порядку идёт 2s. Тоже s и тоже только 2 электрона. 2s2 .
Дальше 2p. Смотрим, сколько электронов может содержать уровень p. 2p6.
Теперь снова возвращаемся на подуровень s, который опять-таки включает в себя всего лишь 2 электрона. 3s2 .
12 уже упорядочено. Осталось 7. И следующий уровень — 3p6.
Остался всего один электрон, который нужно разместить на следующем s-подуровне. В результате на нём остаётся одно свободное место — всего частиц может быть 2, но мы располагаем только одну оставшуюся. А записывается это как 4s1.
В одну строчку это всё записывается следующим образом: 1s2 2s2 2p6 3s2 3p6 4s1.
Важно учитывать, что это электронная конфигурация для основного состояния атома. В Периодической системе элементов у атомов тоже указаны исключительно те их свойства, которыми они обладают в своём основном состоянии
Но также они могут пребывать и в возбуждённом состоянии. Это происходит при сообщении им дополнительной энергии. Тогда электроны с положенных им орбиталей будут перескакивать на другие и запись будет несколько иной.
Валентные и неспаренные электроны
Валентные электроны — электроны, способные участвовать в образовании химических связей.
Представим вкусный большой многослойный ягодный торт. Каждый слой — своего рода уровень. На слоях располагаются ягоды, они же электроны. Но самые вкусные (валентные) всегда располагают сверху на торте. То есть валентные электроны могут быть как на внешнем (в качестве украшения торта), так и на предвнешнем (верхнем бисквитном слое) энергетическом уровне.
Поэтому важно научиться определять количество валентных электронов для различных элементов:
- для элементов главных подгрупп — это все электроны внешнего уровня;
- для элементов побочных подгрупп — это электроны внешнего слоя и предвнешнего d-подуровня.
Среди валентных электронов есть как спаренные электроны, так и неспаренные.
Неспаренными называют электроны, которые находятся поодиночке на орбитали атома, соответственно, спаренные — всегда вдвоем.
Например, у атома водорода один неспаренный электрон на внешнем энергетическом уровне, а вот у атома гелия неспаренных электронов уже нет, но так как оба они находятся на внешнем (и в данном случае единственном) энергетическом уровне, они будут валентными.
Запоминалка: существует последовательность чисел, которая позволяет определить количество неспаренных электронов для атомов главных подгрупп: 1-0-1-2-3-2-1-0.
Таким образом, все неспаренные электроны являются валентными, но не все валентные электроны должны быть неспаренными.
Разберем еще один пример задания №1 ЕГЭ по химии.Задание. Определите, атомы каких из указанных в ряду элементов имеют одинаковое количество неспаренных электронов.1) Li 2) Ca 3) N 4) Ne 5) HРешение. Чтобы решить задание, нужно вспомнить последовательность чисел, которая позволяет определить количество неспаренных электроновдля атомов главных подгрупп: 1-0-1-2-3-2-1-0.Li — элемент IA группы (1-0-1-2-3-2-1-0), значит, у него один неспаренный электрон.Ca — элемент IIA группы (1—1-2-3-2-1-0), значит, у него нет неспаренных электронов.N — элемент VA группы (1-0-1-2-3-2-1-0), значит, у него три неспаренных электрона.Ne — элемент VIIIA группы (1-0-1-2-3-2-1-), значит, у него нет неспаренных электронов.H — элемент IA группы (1-0-1-2-3-2-1-0), значит, у него один неспаренный электрон.Ответ: 15
Строение атома — это тема, с которой всегда начинают познание химии, потому что приступать к изучению химических свойств веществ можно только с пониманием поведения элементарных частиц на атомарном уровне. Изучить тему подробнее и разобрать все ее тонкости поможет статья «Особенности строения электронных оболочек атомов переходных элементов».
Правило Клечковского
Правило Клечковского — по мере увеличения суммарного числа электронов в атомах (при возрастании зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только от главного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра.
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречатреальной энергетической последовательности атомых орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место “провал” электрона с s-подуровня внешнего слояна d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, аименно: после заполнения двумя электронами орбитали 6s следующий электрон появляется на орбитали 5d,а не 4f, и только затем происходит заселение четырнадцатью электронами 4f орбиталей, затем продолжается и завершается заселение десятиэлектронного состояния 5d. Аналогичная ситуация характерна и дляорбиталей 7s, 6d и 5f.
Периодичность свойств элементов. Электроотрицательность
С развитием учения о строении атома, периодический закон занимает ещё больше значимое место в естествознании. Уже неоднократно говорилось, что ПСХЭ является уникальной подсказкой. Достаточно знать расположение и строение электронных оболочек атомов элементов, и возникает возможность судить о том, какими характеристиками он будет обладать. В настоящее время периодический закон имеет формулировку, данную Менделеевым, с небольшим уточнением.

За то, какими свойствами будет наделён элемент, отвечают электроны, которые размещены на внешнем энергетическом уровне. Их ещё называют валентные электроны атома, именно они отвечают за периодическое изменение свойств элементов.
С увеличением массы атома в пределах периода, количество электронов также возрастает, пока не заполнятся все вакантные ячейки уровня.
В ходе химической реакции происходит «движение» электронов. Т.е. одни элементы будут отдавать их, а вторые принимать.
При образовании химических связей, каждый атом стремится «к совершенству», т.е. завершить энергетический уровень. Такой уровень имеют благородные газы ns2np6. А остальным чтобы получить данную конфигурацию необходимо отдать, либо принять электроны.
Рассмотрим на примере, образования вещества NaCl.
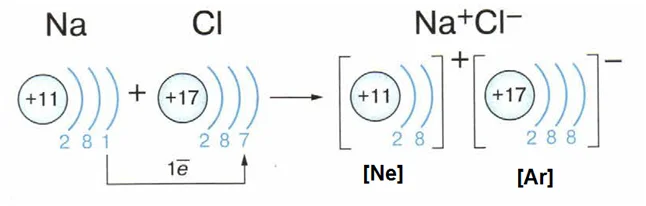
Отдав свой один электрон с внешнего 3s-уровня, атом Натрия образует ион Na+, по своей электронной конфигурации аналогичный Неону. Хлор принимая электрон, образует ион Cl− – принимая электронную конфигурацию Аргона.
Обобщая данный пример, сделаем вывод, элементы, которые содержат малое количество электронов на внешнем уровне (1 – 3) будут только отдавать электроны – и они будут относиться к металлам. Неметаллы характеризуются способностью принимать электроны.

Из определения сделаем вывод, что наибольшую электроотрицательность имеет Фтор (F), нет ни одного элемента, кому бы он смог отдать свой электрон, а будет только забирать. Минимальную ЭО будет иметь Франций (Fr).
Ещё одна важная причина изменения свойств элементов, которая изменяется периодически, это радиус атома. Если ЭО характеризует неметаллы, то по радиусу судят о металлических свойствах. Металлы легко отдают электроны, чем дальше они находятся от ядра, тем легче «отрываются». Радиус атома с увеличением заряда ядра в периоде уменьшается, так как ядро начинает сильнее притягивать электроны.















![Периодическая система элементов и структура электронной оболочки атомов [1972 семишин в.и. - периодическая система химических элементов д. и. менделеева]](http://mse52.ru/wp-content/uploads/d/e/8/de8834ca652dc2b01cba6a13d03611cd.jpeg)





