Как развивалась эпигенетика
Датой зарождения эпигенетики как самостоятельного направления можно считать 1940-е годы. В этот период времени генетик английского происхождения Конрад Уоддингтон предложил термин “эпигенетический ландшафт” и дал ему подробное описание и характеристику.
Смысл этой метафоры состоял в том, что процесс эмбриогенеза напрямую зависит от “ландшафта” скрещивающейся пары, который включает образ жизни и физическое здоровье предыдущих поколений. Один недуг наслаивается на другой, и в результате происходит “изменение ландшафта”, которое приводит к различным генетическим деформациям.
Уоддингтон на протяжении нескольких лет изучал мушек-дрозофил и выяснил следующий факт: если воздействовать на яйца мух высокими температурами, то они рождаются без поперечных жилок в крыльях. При этом, если повторить процесс на протяжении нескольких поколений, то в итоге появится потомство, уже запрограммированное на отсутствие этих жилок без влияния окружающих факторов.
В 1960-х годах ученые пришли к выводу, что не все гены человеческого организма работают по одинаковому принципу. Некоторые из них способны усиливать или увеличивать свое влияние под действием внешних факторов. Но причина этого явления не была до конца понятной.
Новый виток познания вселенной эпигенетики случился в 1998 году. Швейцарским ученым из Университета Базеля удалось проследить интересный феномен: под воздействием высоких температур потомство мух-дрозофил начало рождаться не с желтыми, а с красными глазами. Ученые выяснили, что наследование приобретенных признаков произошло благодаря активации одного-единственного гена, который и менял цвет глаз.
В результате этого опыта появилось понимание того, что стресс как один из сильнейших внешних факторов активирует эпигенетические изменения, которые впоследствие передаются потомству.
Дальнейшие научные опыты подтверждали эту теорию:
-
Ученые из Дюкского университета решили проследить влияние пищевых факторов на дальнейшее потомство. Для изучения этого феномена они добавляли в корм больным ожирением и при этом – беременным мышам полезные элементы (фолиевую кислоту, витамин В12, холин). В итоге у этих мышей родилось абсолютно здоровое потомство.
-
Эндрю Файер и его коллега Крейг Мелло за исследование механизма формирования эпигенетической памяти клеток получили Нобелевскую премию и доказали, что эпигенетика по своим масштабам предполагаемых изменений ничуть не уступает генетике.
Определение эпигенетики
Эпигенетика — это область науки, которая открыла дверь, позволив вам исследовать настоящую причину продолжающихся борьбы и трудностей.
Проще говоря, эпигенетика помогает понять, как функционирует клетка. В свою очередь, это дает представление о том, как возникают проблемы с физическим и психическим здоровьем.
Проблемы с обменом веществ, иммунологические заболевания, болезни сердца, рассеянный склероз, болезнь Паркинсона и другие болезни затрагивают все больше и больше населения. И это не просто небольшой процент людей.
Самая суть того, что движет этими состояниями, с которыми борются так много людей — это проявление информации, хранящейся на клеточном уровне. Этот факт особенно верен в отношении того, во что вы можете верить о себе, сохраняется в ваших клетках в виде организованной материи.
Эпигенетика существенно сместила внимание исследователей и ученых с внешних причин состояний здоровья к изучению того, как самовосприятие закодировано в нашей ДНК. Ваше тело хранит то, что узнает из окружающей среды, на клеточном уровне
Затем это самовосприятие в конечном итоге начинает оказывать глубокое влияние на функционирование ваших клеток.
Они могут включать:
- Регулирование экспрессии генома.
- Транскрипция или копирование генетической информации с ДНК на мРНК (информационная РНК).
- Метилирование, метилированная ДНК — это ДНК, активность которой изменилась, но не ее последовательность.
- Деление клеток, мутации и апоптоз, отсутствие которых может привести к развитию и распространению раковых клеток.
- Производство, ингибирование и регулирование белковых ферментов.
- Регулирование хромосом, особенно у самок млекопитающих.
Эпигенетика признает, что вы являетесь продолжением своего окружения. Кроме того, истинная причина определенных проблем заключается в том, что хранится внутри вас на клеточном уровне.
Ваше тело состоит примерно из 100 триллионов клеток. Они предназначены для одной конкретной цели — впитывать ваш опыт и окружающую среду.
Биологическая догма
Но при всем уважении к классической генетике и ее героям в такой упрощенной картине мира на многое придется закрыть глаза. Легко найти массу примеров тому, как совершенно одинаковые с точки зрения ДНК организмы и клетки получают совершенно разные признаки. Например, у крокодилов, да и вообще у рептилий, нет дополнительной половой хромосомы, как у млекопитающих.
Это, конечно, не деградация хвоста, но уже кое-что довольно близкое. Или — пятнистая окраска кошек: вырастив несколько клонированных котят с полностью идентичными геномами, мы получим совершенно разных на вид животных.
В интернете легко гуглятся фотографии бело-черно-рыжей Рэйнбоу и ее точной копии Сиси с шерстью без единого рыжего или черного пятна. Судя по тому, что клоны радикально не похожи друг на друга, их окраска определяется чем-то еще, помимо самих генов. И ведь это мы еще не вспомнили про разницу взрослого насекомого и личинки, про рабочих пчел и королев…
ДНК — еще не приговор, и догматическая цепочка «ДНК -> РНК -> белок» далеко не так прямолинейна. В конце концов, ведь мы и сами состоим из триллионов клеток, содержащих совершенно одинаковые ДНК, полученные от мамы и папы. Однако наши лейкоциты, эритроциты и нейроны — это «совершенно разные вещи». Каждая клетка организма, как музыкант в оркестре, получает одну и ту же партитуру, но исполняет лишь свою определенную часть, а остальные гены остаются «выключенными».

Старение иммунной системы
Старение связано со снижением функции иммунной системы (иммуносенесценция), что приводит к повышенной восприимчивости как к бактериальным, так и к вирусным инфекциям, злокачественным новообразованиям, аутоиммунным расстройствам и снижению реакции на вакцинацию.
В основном это объясняется изменениями в адаптивном иммунитете, поскольку Т-лимфоциты демонстрируют сниженную иммунную реакцию на антигены и цитотоксическую активность, измененную активность белков секреции и накопление подмножества лимфоцитов памяти, вызванные физиологической инволюцией тимуса. Тимус расположен в верхней части грудной клетки, сразу за грудиной. Кроме того, клетки демонстрируют сниженную выработку высокоаффинных антител и общую неспособность к формированию долговременных реакций памяти. Более того, недавние исследования показали, как старение человека влияет на внутренние компоненты иммунной системы, такие как макрофаги и NK-клетки (естественные киллеры). Поскольку дендритные (вспомогательные) клетки являются наиболее важными антигенпредставляющими клетками, играющими ключевую роль. Функция этих клеток в связи между врожденным и адаптивным иммунитетом, что влияние их поведения на протяжении всей жизни имеет значение.
Эти клетки повсеместно распределены во всех периферических тканях, выполняя роль сторожевых, специализирующихся на поглощении и обработке антигена. После захвата они мигрируют в дренирующие лимфатические узлы, где представляют антигены Т-клеткам, вызывая ответ адаптивной иммунной системы. Во время этой миграции они приобретают несколько фенотипических и функциональных особенностей необходимых для правильной презентации антигена и выделения цитокинов, привлекающих и стимулирующих Т-лимфоциты, а также В-клетки и NK-клетки.
Дендритные (вспомогательные) клетки также являются важнейшими медиаторами иммунной толерантности и анергии, в зависимости от типа антигена, с которым они борются, и от среды, в которой они созревают.
Таким образом, процесс старения в клетке организма.
Связь эпигенетики с внутриутробным развитием
Когда организм развивается в утробе, он имеет свойство адаптироваться к внешним условиям. Если процесс адаптации синхронизировался с условиями после рождения, то информация о предполагаемой угрозе может передаваться следующим поколениям.
Пример: если плод испытывает регулярный дефицит в питании, то в нем срабатывают эпигенетические и метаболические изменения, которые программируют организм на откладывание пищевых ресурсов “на будущее”. Если после рождения плод перестает нуждаться в еде и получает ее достаточное количество, то в будущем несостыковка прошлого и настоящего может привести к диабету или ожирению. Однако такой эпигенетический фактор проявится далеко не сразу, а примерно через 40-50 лет после рождения.
Также эпигенетика очень ярко проявляет себя в психологическом аспекте. Например, нервная система детей, которые не чувствовали родительскую любовь или подвергались насилию, вследствие деформируется и искажается. В 90% случаев эти изменения стабильно закреплены в клетках мозга и в дальнейшем очень ярко дадут о себе знать.

Интересуетесь антивозрастной
и превентивной медициной?
Узнайте больше на обучающих программах Anti-Age Expert

Чтобы стать лучшим — учитесь
у лучших!
Эксперты со всего мира станут вашими наставниками
на пути изучение Anti-Age Expert. Подробнее
Список литературы
- Waddington C.H. Canalization of development and the inheritance of acquired characters.
- Nieratschker V., Batra A., Fallgatter A. (2013). Genetics and epigenetics of alcohol dependence.
- Anway M.D., Cupp A.S., Uzumcu M., Skinner M.K.Epigenetic transgenerational actions of endocrine disruptors and male fertility.
Эпигенетика и unstable repeats
В некоторых частях ДНК есть так называемые нестабильные повторения, когда небольшая последовательность нуклеодитов многократно повторяется . Считается, что в некоторых частях ДНК механизмы починки и репликации «соскальзывают», давая подобные повторения .
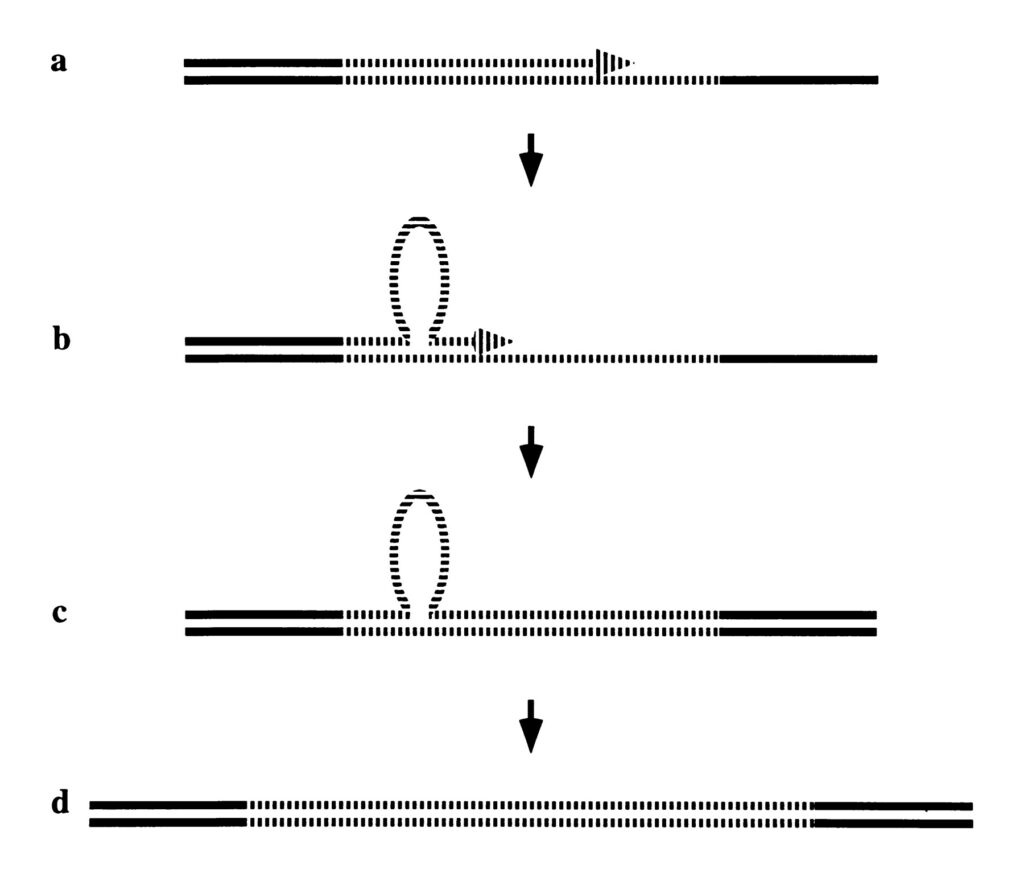
Проблема нестабильных повторений в том, что они с поколениями могут увеличиваться . Увеличение unstable repeats с поколениями называется anticipation.
Unstable repeats, HTT ген и хорея Гентингтона
Хорея Гентинтона – в основном генетическая болезнь. Белок huntingtin, роль которого в развитии профильного заболевания толком не ясна, кодирует ген HTT, находящийcя в позиции 4p16.3 (короткая «ручка» 4-й хромосомы). Когда число повторений становится слишком большим – белок теряет свою функцию, и последующие поколения постепенно приходят к болезни Гентингтона.
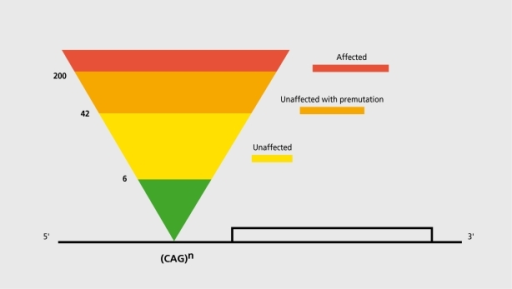
Обычно есть такая пирамида, в случае хореи Гентингтона это:
- Доброкачественная (benign) вариация – Меньше 26 повторений CAG;
- Промежуточная (intermediate) вариация – 27 – 35 повторений CAG;
- Пре-мутация – 36-40 повторений CAG;
- Патологическая мутация – больше 40 повторений CAG
Может ли эпигенетика включать наследуемую патологию роста количества нестабильных повторений в HТТ гене? Будем считать, что я много могу себе позволить в собственной же заметке.
Связь разума и тела
Эпигенетические исследования показывают, что выбор образа жизни можно напрямую проследить до генетического уровня, доказывая, что связь разума и тела неоспорима.
У всех нас есть выбор в том, какую информацию получат наши клетки, положительную или отрицательную.
Есть разные способы подойти к жизни. Это либо из страха и сомнений, либо из любви и принятия. Что бы вы ни выбрали, это может сильно повлиять на ваше тело. Неудивительно, что страх и сомнения могут уступить место тревоге, депрессии и гневу, которые захватят нашу жизнь.
Из места любви и веры мы растем позитивно. Положительные эмоции, такие как любовь, привязанность, радость и уверенность, помогают нам стать лучше и узнать, кто мы есть на самом деле. Ваше мышление распознается и понимается вашим телом, вплоть до генетического уровня. Ваши мысли действительно обладают удивительной силой влиять на вашу физиологию.
Ваши мысли программируют ваши клетки. Мысль — это нейрохимическое событие, которое сигнализирует о ряде химических и электрических частиц в форме нейро- или полипептидов.
Затем эти полипептиды ищут рецепторные участки на клетках. Каждая ячейка содержит тысячи и тысячи рецепторных ячеек, и эти ячейки предназначены для получения информации.
Если мы наводним стволовые клетки неверной информацией, то дочерние клетки, образованные в результате митоза, структурно изменятся. Эти структурные изменения могут привести к ряду физических и психических проблем.
По мере развития технологий наука показывает, что мы только начинаем понимать сложную связь разума и тела. Проще говоря, чем больше вы улучшите свои умственные привычки и поощряете позитивное, правдивое мышление, тем больше пользы получит ваше тело.
Основные эпигенетические механизмы
Эпигенетика изучает наследуемые свойства организма. Самое главное в том, что эти свойства не связаны с изменением последовательности нуклеотидов ДНК. То есть речь идёт не о мутациях, а о механизмах, которые «включают» или «выключают» гены.
Метилирование ДНК
Метилирование — это присоединение метильной группы CH3 к цитозину в последовательностях нуклеотидов «цитозин — гуанидин» (CpG). Происходит оно с помощью фермента метилтрансферазы.
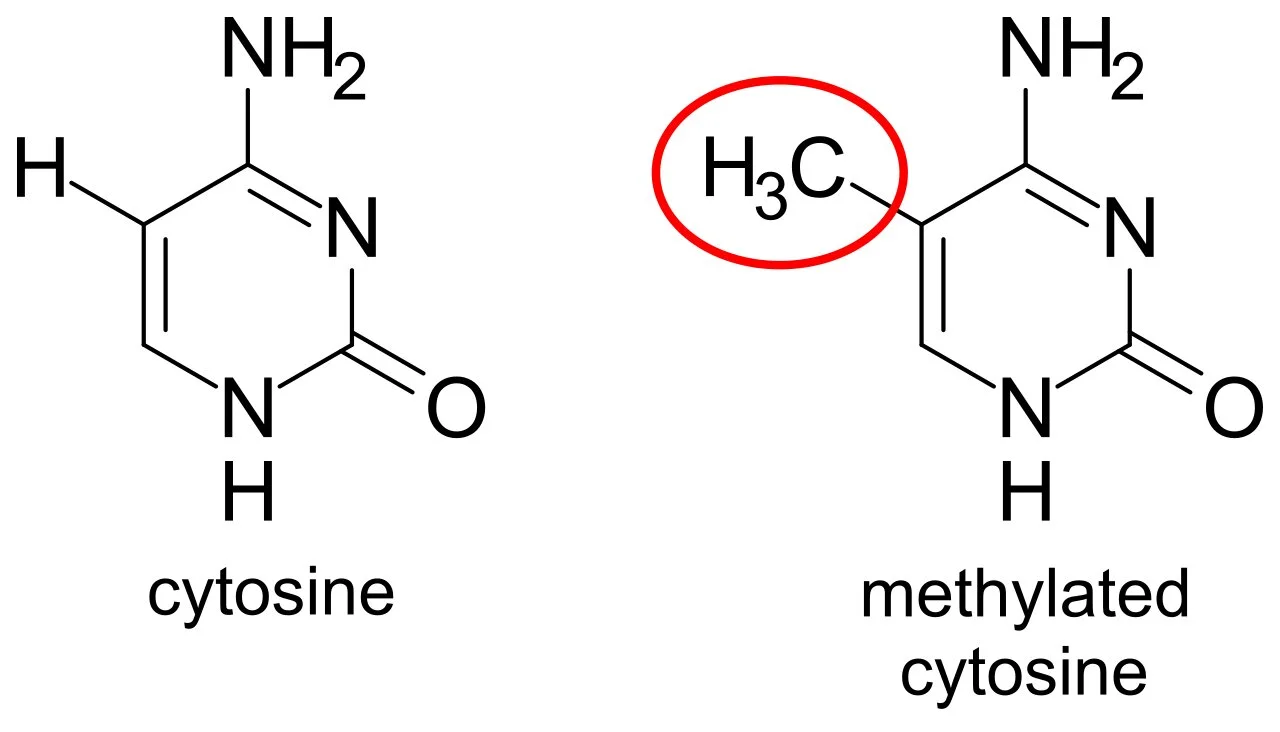 Метилирование цитозина — присоединение метильной (CH3) группыCytosine — цитозин, methylated cytosine — метилированный цитозин
Метилирование цитозина — присоединение метильной (CH3) группыCytosine — цитозин, methylated cytosine — метилированный цитозин
Примерно 70% промоторов в геноме человека насыщены этими последовательностями, а всего метилирован 1% геномной ДНК. Метильные группы не дают транскрипционным факторам присоединиться к ДНК, а значит, транскрипция останавливается.
Обратный процесс — отсоединение метильной группы — называется деметилирование. Оно снимает запрет на транскрипцию.
Что интересно, у млекопитающих во время удвоения ДНК новая цепь тоже метилируется. А значит, оно сохраняется после деления клетки.
Модификация гистонов
Длина ДНК составляет 1,5 — 2 метра, при этом она умещается в ядро клетки. Дело в том, что ДНК, словно на катушку, намотана на белки гистоны. Гистоны заряжены положительно, а ДНК отрицательно, это помогает её зафиксировать.
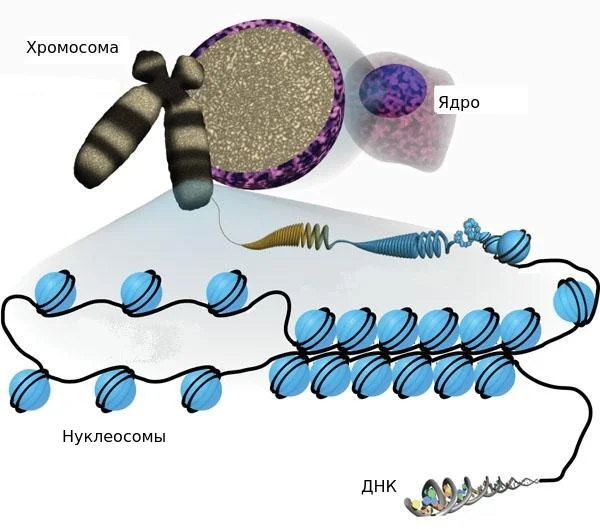 Гистоны и «намотанная» на них ДНК образуют нуклеосому
Гистоны и «намотанная» на них ДНК образуют нуклеосому
Перед транскрипцией связь с гистонами ослабляется и ДНК становится доступной для РНК-полимеразы и транскрипционных факторов.
У гистонов есть фрагменты, выступающие наружу, это так называемые «гистоновые хвосты». Специальные ферменты прикрепляют к гистонам химические группы: метильные, ацетильные, фосфатные и другие, а также небольшие белки (убиквитин, SUMO). Получаются гистоновые метки.
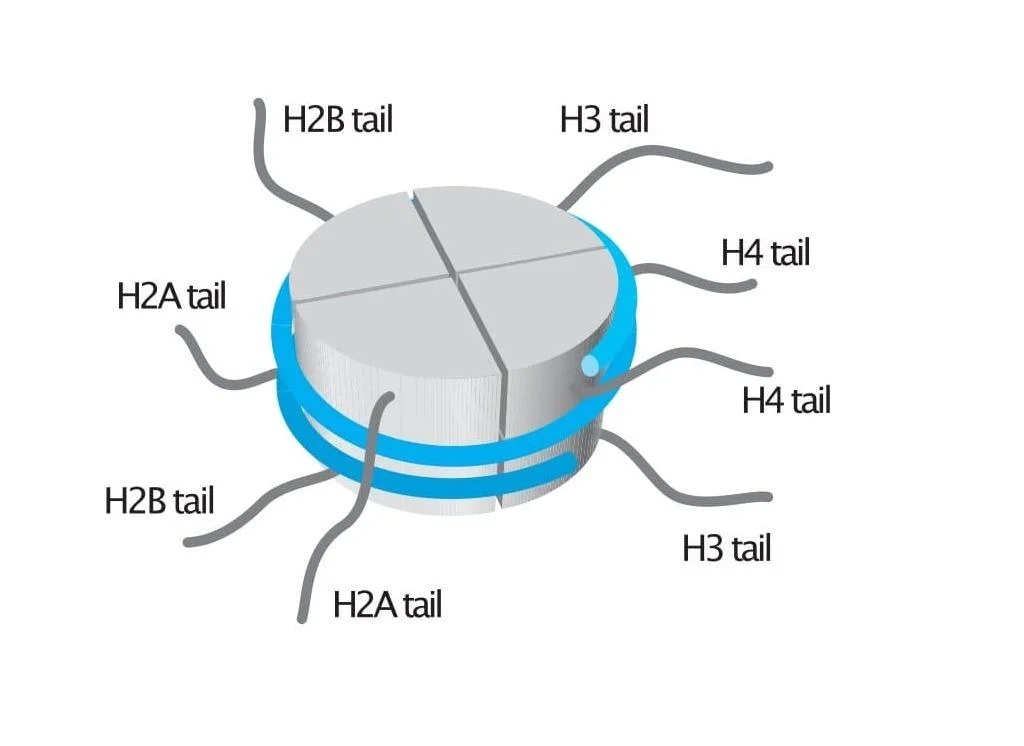 Нуклеосома: комплекс из нескольких гистонов (серый цвет), вокруг которого ДНК (голубой цвет) делает 2,5 оборота. От гистонов отходят хвосты (tail — хвост)
Нуклеосома: комплекс из нескольких гистонов (серый цвет), вокруг которого ДНК (голубой цвет) делает 2,5 оборота. От гистонов отходят хвосты (tail — хвост)
Присоединение остатка уксусной кислоты называется ацетилирование. Оно снижает заряд гистонов и тем самым ослабляет связь между ними и ДНК. Это помогает начать транскрипцию. Обратный процесс — деацетилирование (удаление остатков уксусной кислоты) — тормозит транскрипцию.
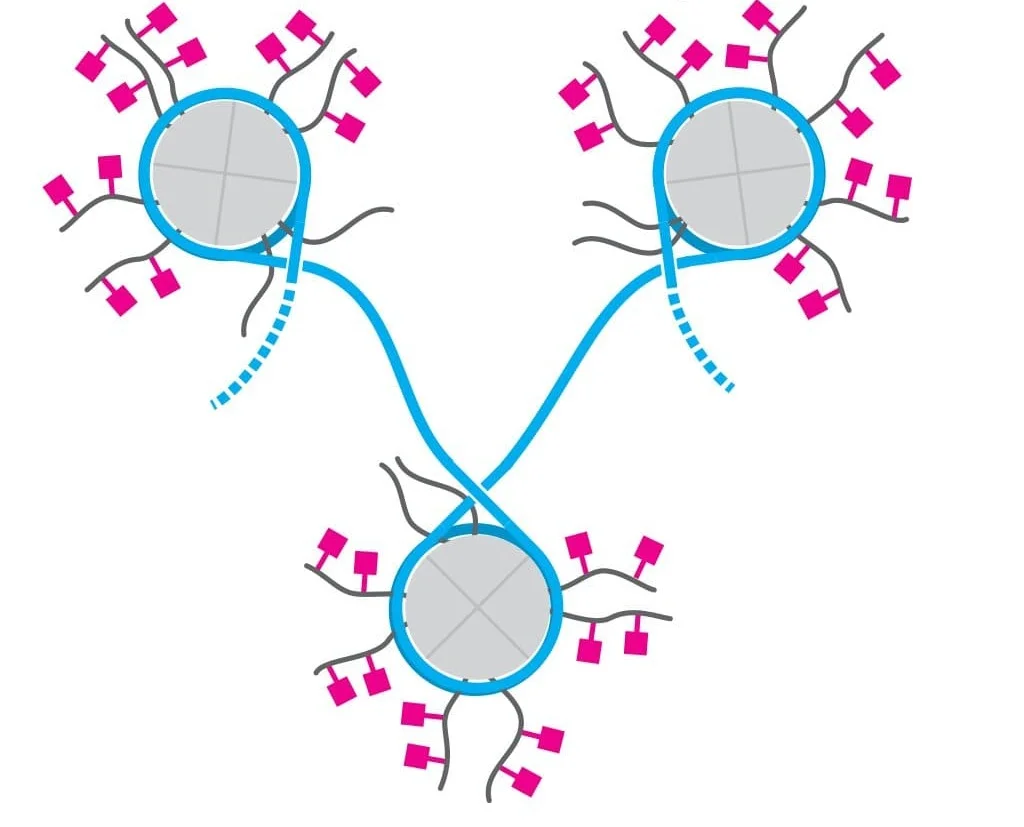 Розовым цветом обозначены остатки уксусной кислоты, присоединённые к гистоновым хвостам
Розовым цветом обозначены остатки уксусной кислоты, присоединённые к гистоновым хвостам
Присоединение фосфатной группы — фосфорилирование — усиливает отрицательный заряд гистонов. ДНК тоже заряжена отрицательно, следовательно, отталкивание между гистонами и ДНК усиливается. Белки, ответственные за транскрипцию, легче прикрепляются к ДНК, а значит, транскрипция ускоряется.
Когда синтезируется новая нить ДНК, «старые» модифицированные гистоны встраиваются в новые нуклеосомы. Однако гистоны в нуклеосомах заменяются и модификации постепенно пропадают. Исследователи ещё изучают, на протяжении какого количества делений передаются модификации гистонов.
Эпигенетика: новая дисциплина
Так родилась новая дисциплина – эпигенетика (над, или сверх генетики). Один из тех, кто занимается исследованием этого интригующего механизма, доктор Бас Хейманс, говорит:
Нейробиолог Тель-Авивского университета Одед Рехави заявил:
Исследования, указывающие на изменения в доступе к генетической информации в ДНК (генотип), вызванные внешними или экологическими стимулами и приводящие к изменениям в организме (фенотип), множатся. Эксперименты проводились на червях:
В другом примере РНК-глушитель, индуцированный в червях в ответ на введенный вирус, продолжал экспрессироваться на протяжении более 100 поколений.
Исследования костей бизона, найденных в вечной мерзлоте на канадском золотом прииске, показали, что эпигенетические изменения в популяции бизонов позволили им быстро адаптироваться к изменениям климата. Эти изменения слишком быстры, чтобы их можно было объяснить традиционными дарвиновскими моделями естественного отбора.
Ученые, проводившие эксперименты на мышах агути, обнаружили, что, манипулируя питанием, они могут выключить определенный ген. Когда ген активен («включен»), мыши обычно страдают ожирением и имеют желтоватый цвет; при выключении гена мыши становятся нормальными, стройными и коричневыми. Если перед спариванием кормить мать комбинацией питательных веществ, включая витамин B12, ген удавалось выключить у малышей.
 Изогенные мыши агути одного возраста и пола. Цвет шерсти и ожирение зависят от эпигенетического статуса определенного аллеля.
Изогенные мыши агути одного возраста и пола. Цвет шерсти и ожирение зависят от эпигенетического статуса определенного аллеля.
Эволюционисты, придерживающиеся парадигмы современного синтеза (неодарвинизм; мутации и естественный отбор объясняют разнообразие жизни на Земле), как правило, оказывают сильное сопротивление выводам, полученным в результате эпигенетических исследований. По их мнению, эволюция – это медленный процесс случайных мутаций в геноме, приводящий иногда к крошечному преимуществу в фенотипе. Ему благоприятствует естественный отбор, и оно передается по менделевской наследственности будущим поколениям.
Ген рассматривается как хозяин, контролирующий внешнее проявление в клетке и более крупном организме. Эта идея стала популярной в книге Докинза «Эгоистичный ген». Идея о том, что взаимодействие внешней формы организма с окружающей средой передает информацию обратно в геном или даже просто влияет на то, как геном «действует», является для них анафемой.
Что еще хуже для эволюционистов, эпигенетика предполагает, что скрытая генетическая информация сидит в ДНК в ожидании определенной среды, чтобы быть включенной или выключенной. Это похоже на информацию в книге с определенными страницами, скрепленными вместе, которые должны быть открыты, чтобы информация начала действовать в определенных условиях окружающей среды.
Если эволюция происходит путем естественного отбора, когда окружающая среда отбирает или сохраняет эффект случайных мутаций, то как может существовать «набор» генетической информации, который только и ждет, чтобы быть включенным средой, которой организм еще не подвергался? Это добавляет еще одну загадку типа «курица или яйцо» к тем многочисленным примерам, которые уже бросают вызов эволюционистам.
Наследование эпигенетических отпечатков
Открытия эпигенетических изменений, особенно в популярной науке, постоянно проводят параллели с ламаркизмом. Ламаркизм, или передача приобретенных характеров, рассматривается как противоречащий классической генетике.
Однако существует очень мало доказательств того, что приобретенные и приобретенные способности могут передаваться через половые клетки. Передача приобретенных способностей следующему поколению еще не является доказательством генетического проявления. Кроме того, термин «поколение» часто неверно истолковывают как начало индивидуального цикла.
Наследование эпигенетических отпечатков было предложено в 2003 году Рэнди Джиртлом и Робертом Уотерлендом с использованием экспериментов на мышах. Самкам мышей агути перед спариванием и во время беременности вводили определенный состав питательных веществ. Было обнаружено, что большая часть потомства не проявляла типичного фенотипа.
В исследовании на людях различные факторы, предоставившие информацию о доступности пищи и смертности в маленьком шведском городке Оверкаликс . Было обнаружено, что у большинства людей, чьи бабушки и дедушки резко изменили рацион питания, с возрастом развивались сердечно-сосудистые заболевания.
Однако болезнь развивалась по определенной схеме, которая предполагает эпигенетические изменения в половых хромосомах. Например, в семьях, где дедушка ел хорошо или слишком много, пострадали только внуки мужского пола.
Согласно гипотезе Уильяма Р. Райса и его коллег, эпигенетика может быть причиной человеческого гомосексуализма . Сексуальное предпочтение матери будет передано сыну, а предпочтение отца — дочери.
Это могло бы произойти, если бы эпигенетические маркеры генов, ответственных за сексуальную ориентацию, сохранялись в половых клетках. Если не удалить эпигенетические метки в яйцеклетке, эмбрион может иметь сексуальную ориентацию матери. Согласно этой гипотезе, гомосексуализм у человека врожденный.
Гипотеза объясняет, почему случаи гомосексуализма у людей остаются статистически стабильными с течением времени. Однако нет никаких эмпирических доказательств связи между гомосексуализмом и эпигенетикой.
Изменение негативных убеждений и поощрение позитивного мышления
Участие в позитивной психической практике самообслуживания абсолютно необходимо для поддержания оптимального физического и психического здоровья. Превращение негатива в позитив способствует самым благоприятным изменениям в организме.
Вы не можете контролировать большинство внешних событий, которые происходят в жизни, но вы можете контролировать свое восприятие этих событий. Ваше восприятие себя и происходящих событий имеет ключевое значение.
Ваше мышление играет роль в формировании неврологической проводки. Это касается, в первую очередь, того, как ваши клетки запрограммированы и как ДНК выражает себя.
Предоставляя своим клеткам правильную информацию и положительное, точное восприятие, вы можете изменить свой мозг, клетки и гены. Это помогает устранить или, по крайней мере, значительно уменьшить проблемы с психическим и физическим здоровьем.
Ваши клетки умны. Они знают, кто они и что им нужно, чтобы хорошо функционировать.
Однако это не означает, что они задаются вопросом, какую информацию они получают. Они работают с тем, что им дают, будь то положительное или отрицательное.
«Традиционные» представления о работе ДНК
Речь пойдёт о генах эукариот, так как эпигенетика начиналась с исследования эукариотических организмов.
Структура гена у эукариот
Ген — это участок ДНК, который кодирует белок или РНК.
Его основные элементы:
- Промотор — участок ДНК, к которому присоединяется фермент РНК-полимераза, которая будет синтезировать РНК.
- Кодирующая последовательность, которая несёт информацию о белке. На её основе и собирается РНК.
- Терминатор — участок ДНК, на котором останавливается синтез РНК.
Существуют энхансеры и сайленсеры — участки ДНК, которые влияют на ход транскрипции.
- Энхансер (англ. enhancer — усилитель) повышает активность транскрипции.
- Сайленсер (англ. silenser — глушитель) снижает активность транскрипции.
Энхансеры и сайленсеры не обязательно находятся в области промотора, они могут быть «рассеяны» вокруг гена.
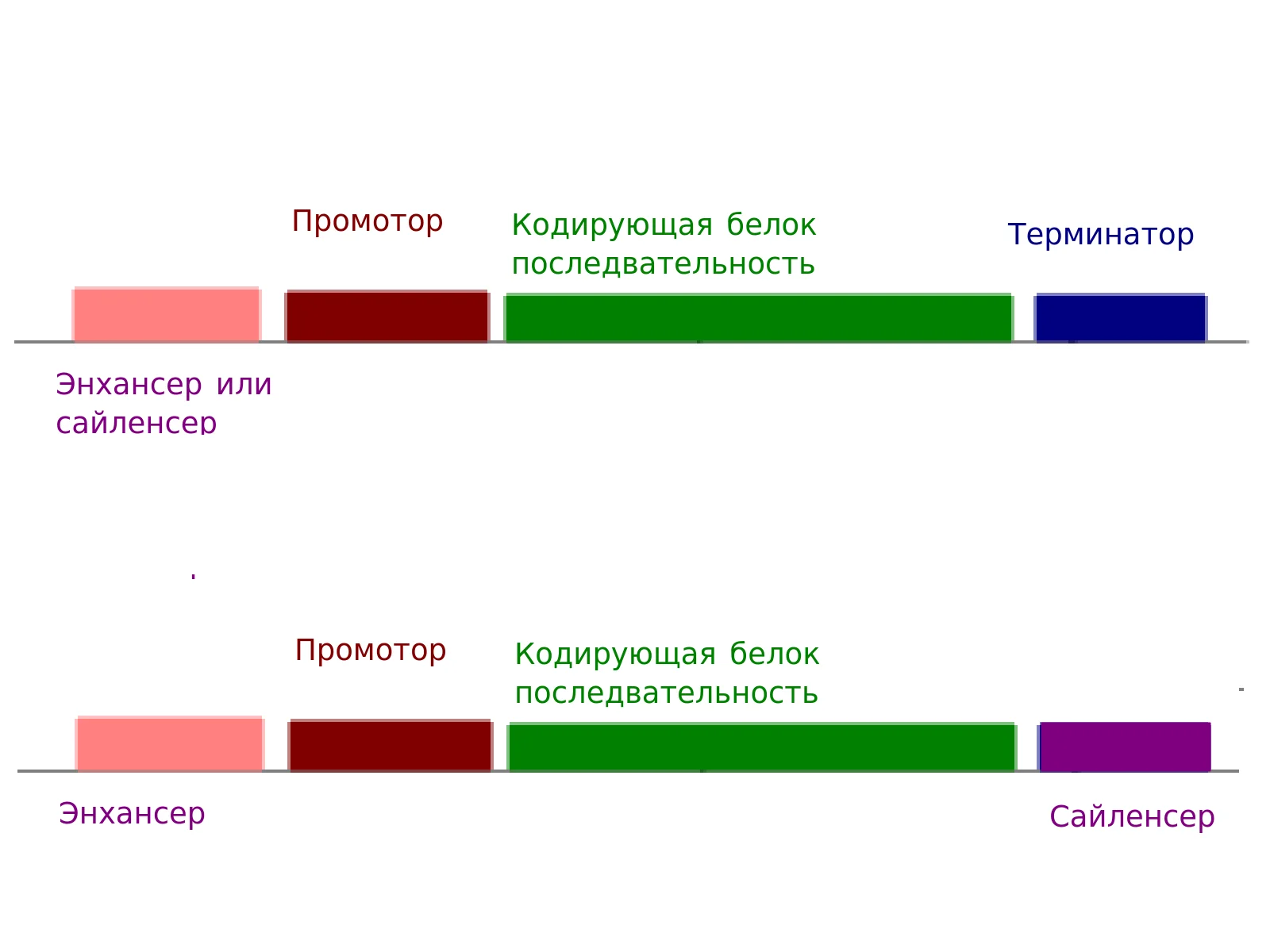 Варианты строения гена
Варианты строения гена
Ход транскрипции
Считывание генетической информации происходит по следующему сценарию:
- Перед считыванием гена нужный участок ДНК «расплетается».
- Фермент РНК-полимераза на основе нуклеотидных последовательностей гена синтезирует информационную РНК.
- На основе информационной РНК рибосомы собирают белок.
Кроме понятия «транскрипция гена», существует термин «экспрессия гена». Экспрессия — это выражение, то есть «выражение гена». Если с гена происходит считывание информации (накапливается информационная РНК и белок), то говорят, что происходит экспрессия гена. Другими словами, «экспрессия» — это синоним «активности» гена.
Гены разделяют на структурные и функциональные. Структурный ген кодирует последовательность аминокислот белка. Функциональные гены регулируют работу структурных генов.
Для того, чтобы РНК-полимераза синтезировала РНК, ей необходимы дополнительные белки — транскрипционные факторы. Они связываются с участком ДНК перед началом транскрипции и регулируют её. Существуют белки, которые не взаимодействуют с самой ДНК, но тоже влияют на транскрипцию. Это коактиваторы, корепрессоры, медиаторы.
Гормоны выполняют роль регуляторов транскрипции. Под их действием усиливается синтез белков. Самый яркий пример — это стероидные гормоны: кортизол, альдостерон, половые гормоны.
Стероидный гормон проходит через мембрану клетки. Внутри клетки он связывается с рецептором, так образуется комплекс «гормон — рецептор». Затем комплекс «гормон-рецептор» погружается внутрь клетки и доходит до ядра. И уже в ядре он запускает транскрипцию генов.
Схема действия стероидных гормонов
1 — гормон соединяется с рецептором;
2 — образуется комплекс «гормон — рецептор»;
3 — комплекс «гормон — рецептор» регулирует транскрипцию белка.
Эпигенетические изменения при старении
Существуют различные типы эпигенетической информации, закодированной в наш эпигеном, включая, но не ограничиваясь наличием или отсутствием гистонов на какой-либо конкретной последовательности ДНК.
Все больше свидетельств в последние годы также явно указывают на структуру хроматина, который несет много эпигенетической информации, как основного игрока в процессе старения. Основная единица структуры хроматина является нуклеос, который состоит из 147 пар оснований ДНК обернутых вокруг гистонов. Упаковка геномной ДНК в высокоорганизованную структуру хроматина регулирует все геномные процессов в ядре, в том числе репликацию ДНК, транскрипцию, рекомбинацию и репарацию ДНК, контролируя доступ к ДНК.
Исследования на людях и различных моделей деградации свидетельствуют о прогрессирующей потери конфигурации при старении хромосомной архитектуры, целостность генома и экспрессия генов. Исследования подтвердили, что все эти эффекты в основном сохраняется на всем пути от одноклеточных организмов, таких как дрожжи, до сложных многоклеточных как человек. Эти сохраняющиеся механизмы помогают получить более четкое представление о процессе старения. Эпигенетические изменения в значительной степени влияют на процесс старения для последующих достижений в области эпигенетики и выявления возможных перспективных направлений.
Сокращение гистона при старении
Репликативное нарушение сопровождается потерей примерно половина основных гистоновых белков.
Резкое снижение основных гистоновых белков обусловлено снижением синтеза белков гистонов. У человека, снижение синтеза новых гистонов во время деградации является следствием роста укороченной длины теломера, которые активируются в ответ на повреждение ДНК, потенциально объясняя механизм укорочения теломер ограничением числа делений клеток. Следовательно, потери основных гистонов может быть более обобщенное явление, наблюдаемое с возрастом у многих организмов.
Процесс старения, несомненно, является сложным. В организме жизни, старение клетки претерпевает множество изменений и происходит накопление повреждений макромолекул. Фенотип старения проявляется путем суммирования изменений различных сигналов.
Генетические и экологические изменения однозначно важно расшифровать для действия конкретного фактора на процесс долголетия. Становится очевидным механистически, что многие из тех факторов, которые влияют на продолжительность жизни, действуют главным образом путем модификации эпигенома
Несомненно, эпигенетическое влияние на процессы старения должны быть включены в нашем нынешнем понимании старения.
Старение клетки
Молодые здоровые клетки поддерживают эпигенетическое состояние, что способствует образованию компактной структуры гистона и регуляции основных биологических процессов. Однако старение клетки испытывают изменения во всех аспектах. Обратимый характер эпигенетических механизмов позволяет восстановить или обратить вспять некоторые из этих фенотипов для достижения более молодой клетки. В то время как некоторые молекулярные изменения при старении могут быть классифицированы как причина старения, другие изменения просто сопровождают процесс старения. Однако, характеризуя причины и последствия деградации, нужно внимательно проанализировать экспериментальные результаты, поскольку большинство соответствующих путей взаимосвязаны.
Постоянное сочетание функционального анализа и молекулярного анализа в разных возрастных группах, у разных организмов и разных типах тканей даст всю необходимую информацию чтобы постичь этот эволюционно законсервированный основной процесс с целью разработки терапевтических мероприятий, чтобы противодействовать возраст-индуцированным осложнениям. Центральное понятие складывается для разработки эпигенетических препаратов или даже эпигенетического питания.
Таким образом, основные проблемы, которые будут доминировать на поле в ближайшем будущем будет достижение иерархического понимания того, как эпигенетика влияет на процесс старения и понимание долгосрочных эффектов лечебных вмешательств на эпигеном в стареющем человеке, учитывая взаимосвязанность эпигенетических механизмов.
Несколько важные выводы вытекают из этих исследований: генетическая предрасположенность старения 20-30 %, а остальное в нашей жизни во многом определяется питанием и другими воздействиями внешней среды.
C сравнение к генетике
Термин эпигенетика можно понять, если рассмотреть процесс наследования:
- Перед делением клетки генетический материал удваивается. Затем половина дублированного генома переносится в одну из двух дочерних клеток. Половина материнского генетического материала доставляется яйцеклеткой, а отцовская половина — сперматозоидом.
- Молекулярная генетика описывает генетический материал как двойную спираль двух цепей дезоксирибонуклеиновой кислоты. Нити содержат фосфат-дезоксирибозный сахарный полимер в качестве основы. Генетическая информация поступает из последовательности четырех оснований, которые присоединены к остову сахара дезоксирибозы. Это аденин (A), цитозин (C), гуанин (G) и тимин (T).
- Основания одной нити почти всегда сочетаются с совпадающим основанием второй нити. Аденин соединяется с тимином, а цитозин — с гуанином.
- Генетическая информация закрепляется в порядке строительных блоков A, C, G, T (базовая последовательность).
Некоторые явления наследственности нельзя объяснить с помощью только что описанной модели ДНК:
- Во время дифференцировки клеток в процессе деления клеток образуются дочерние клетки с другой функцией. После дифференцировки клеток разные типы клеток все еще сохраняют сходные последовательности ДНК. Определение функциональной идентичности клетки — тема эпигенетики.
- Есть черты, которые «унаследованы» только от отца или матери и не связаны с ДНК. Нарушения этого состояния приводят к серьезным заболеваниям.
- Когда дифференцированные клетки снова трансформируются в стволовые, эпигенетические паттерны должны быть удалены. Клетка может снова приобрести и унаследовать все или многие функции, когда эпигенетические фиксации удалены.
Биологическая предрасположенность старения
Старение организма — сложный многофакторный биологический процесс, общий для всех живых организмов. Он проявляется постепенным снижением нормальных физиологических функций в зависимости от времени
Биологическое старение организма имеет важное значение для здоровья человека, потому что с возрастом увеличивается восприимчивость ко многим болезням, включая рак, метаболические расстройства, такие как диабет, сердечно-сосудистые нарушения и нейродегенеративные заболевания. С другой стороны, старение клеток, также называемое репликативная деградация, является специализированным процессом и рассматривается как потенциальный эндогенный противоопухолевый механизм при котором происходит необратимый рост потенциальных онкогенных стимулов
Клеточное старение носит много общего с процессом старения, но и показывает отличительные черты. Хотя причины старения недостаточно изучены, продолжаются усилия, чтобы очертить пути долголетия.
В последние годы большие успехи достигнуты в ходе многочисленных исследований, что эффективно проявляется на клеточных и молекулярных признаках старения. Среди этих признаков эпигенетические изменения являются одними из важнейшим механизмов ухудшения функции клеток, наблюдаемые при старении и возраст-зависимых заболеваний.
По определению эпигенетика представляет обратимый наследственный механизм который происходит без какого-либо изменения базовой последовательности ДНК, а также происходит репарация ДНК.
Хотя хромосомы в геноме несут в себе генетическую информацию, эпигеном, ответственным за функциональное использование и стабильность является генотип с фенотипом – общими характеристиками. Эти эпигенетические изменения могут быть спонтанными или под влиянием внешних или внутренних воздействий. Эпигенетика потенциально служит недостающим звеном, чтобы объяснить, почему картина деградации отличается от двух генетически идентичных особей, таких, как однояйцовые близнецы, или же, в животном мире, между животными с одинаковой генетической структурой, например, матки и рабочих пчел.
Например, различные дифференциальные изменения хранимой эпигенетической информации создает поразительный контраст во внешности, репродуктивном поведении и продолжительности жизни рабочих пчел и матки, несмотря на идентичное содержание ДНК.
Таким образом, эпигенетика открывает большие перспективы для выбора лечебных мероприятий при генетических изменениях, которые в настоящее время технически необратимы в организме человека. Соответственно, определение и понимание эпигенетики и эпигенетических изменений, которые происходят во время старения, является основной областью исследования, которое может проложить путь к разработке новых терапевтических подходов к задержке старения и возрастных заболеваний.






























