Строение жидкого вещества
Если уменьшать температуру газа, то энергия молекул будет всё меньше, свободный пробег — тоже. Наконец, молекулы в среднем станут находиться настолько близко друг к другу, что силы притяжения начнут играть заметную роль в поведении вещества, выражаясь в виде поверхностного натяжения. Сила тяжести будет также вносить свою лепту: в результате вещество займет нижнюю часть предоставленного объема.
В жидком состоянии молекулы находятся очень близко друг к другу. Поэтому сжать их можно лишь за счет изменения формы молекул, для чего требуется гораздо больше энергии по сравнению со сжатием за счет уменьшения расстояний между молекулами. Большую часть времени молекулы жидкости проводят в беспорядочных колебаниях, но появление даже небольшой внешней силы способно двигать молекулы жидкости, что обеспечивает текучесть.
Рис. 2. Молекулы в жидкости.
Строение газа
При достаточно высокой температуре и не слишком большом давлении молекулы вещества обладают большой энергией, и сил их взаимодействия недостаточно, чтобы удерживать их рядом. Сила гравитации также оказывается недостаточной, чтобы заметно влиять на поведение молекул. Поэтому при таких условиях молекулы могут свободно перемещаться в пространстве, заполняя весь предоставленный объем.
Молекулы сталкиваются друг с другом и с другими телами, создавая давление газа, однако путь их свободного полета многократно превышает размеры молекул. Взаимодействия происходят лишь в короткое время столкновения. Связь давления с объемом и температурой описывается газовыми законами.
Рис. 1. Три газовых закона.
Движение молекул
Будет ли чай в стакане сладким, если сахар в нем не перемешивать? Да, конечно. Но через определенное время, за которое молекулы сахара со дна стакана поднимутся в верхние слои жидкости. Значит, молекулы движутся. Как они движутся и где?
Простой опыт:
Если в полстакана крупы засыпать без перемешивания полстакана гороха, получится целый стакан. Крупинки и горошинки небольшие, но не могут «протиснуться» в пустые промежутки.
А если в мензурку налить по одинаковому количеству воды и спирта? Увеличения смеси в два раза, как в первом случае, не получится. Почему? Молекулы воды и спирта совершенно разные. Между молекулами воды расстояния больше, чем между молекулами спирта. Вот эти промежутки частично и заполняются, уменьшая объем смеси.
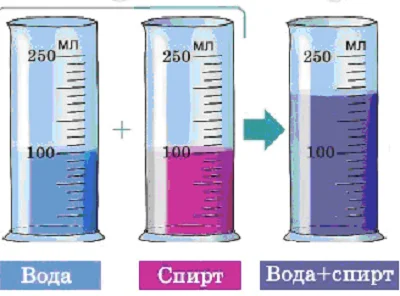
Таким же образом молекулы сахара «разбегаются» по всему объему, делая чай сладким.
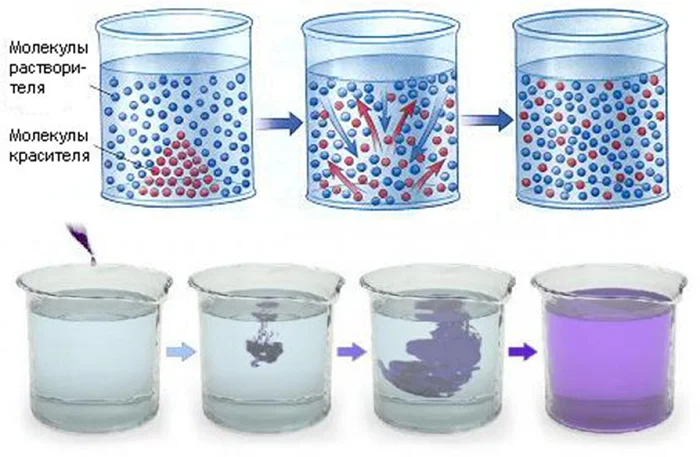 (Источники и )
(Источники и )
Проникновение молекул одного вещества в промежутки между молекулами другого называется диффузией.
В газах диффузия – тоже довольно частый процесс. Проходя мимо кондитерской фабрики, люди наслаждаются запахом карамели, зефира, шоколада, входя в парикмахерскую, ощущают аромат духов, одеколона, туалетной воды. Человека постоянно сопровождают запахи. Они несут важную информацию о веществе, благодаря диффузии. В газах она протекает быстрее, чем в жидкостях, и вот почему. Межмолекулярные расстояния в газах больше, чем в жидкостях, отсюда возможности для движения больше.
А возможна ли диффузия в твердых телах? Нужно учитывать, что твердое тело держит форму без изменения, благодаря расстояниям, близким к размерам самих молекул или даже меньше их. Могут ли туда проникнуть «чужие» молекулы? Оказывается, диффузия в твердых телах тоже возможна, но при условии, что они находятся в очень тесном контакте друг с другом. Процесс длится очень медленно, и время измеряется годами. Известен опыт с двумя отшлифованными телами из золота и свинца. Их плотно прижали друг к другу и оставили под наблюдением. Диффузия произошла. Всего на 1 мм за пять лет.
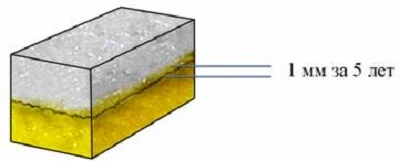 (Источник)
(Источник)
Движение молекул и промежутки между ними объясняют диффузию. Гипотезу об этом впервые высказал греческий ученый Эпикур в III веке до н.э.
Опытным путем доказал это в 1827 г. Броун, знаменитый английский ботаник. Он рассмотрел через микроскоп споры растения плаун, находящегося в воде, и заметил, что эти маленькие частички постоянно двигаются в разных направлениях. Безостановочное, беспорядочное движение продолжалось и днем, и ночью, в любое время года. Почему же двигались споры растения? А двигались они потому, что их толкали и заставляли двигаться невидимые в простой микроскоп молекулы воды.
Молекулы движутся постоянно, сближаются друг с другом и, отталкиваясь, приобретают новое направление движения. Их много в веществе, и встречи, изменяющие направление, происходят очень часто. Суммарный удар нескольких молекул приводит в движение небольшие частицы, попавшие в воду. Движение этих частиц назвали броуновским движением, а сами частицы – броуновскими.
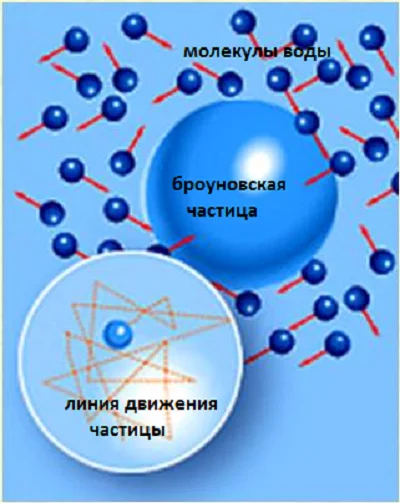 (Источник)
(Источник)
Итак, следует запомнить:
- Между молекулами существуют промежутки
- Молекулы движутся хаотично и постоянно
- Явление проникновения молекул одного вещества в промежутки между молекулами другого называется диффузией.
Строение вещества
- Подробности
- Обновлено 17.08.2018 14:30
Все вещества состоят из отдельных мельчайших частиц : молекул и атомов.
Основоположником идеи дискретного строения вещества (т.е. состоящего из отдельных частиц) считается древнегреческий философ Демокрит, живший около 470 года до новой эры. Демокрит считал, что все тела состоят из бесчисленного количества сверхмалых, невидимых глазу, неделимых частиц. «Они бесконечно разнообразны, имеют впадины и выпуклости, которыми сцепляются, образуя все материальные тела, а в природе существуют только атомы и пустота.
Догадка Демокрита была надолго забыта. Однако, его взгляды на строение вещества дошли до нас благодаря римскому поэту Лукрецию Кару: «… все вещи, как мы замечаем, становятся меньше, И как бы тают они в течение долгого века…»
Атомы
Атомы очень малы. Их невозможно разглядеть не только простым глазом, но и с помощью даже самого мощного оптического микроскопа.
Глаз человека не способен разглядеть атомы и промежутки между ними, поэтому любое вещество кажется нам сплошным.
В 1951 году Эрвин Мюллер изобрёл ионный микроскоп, позволивший в деталях разглядеть атомную структуру металла.
Атомы различных химических элементов отличаются друг от друга. Различия атомов элементов можно определить по периодической таблице Менделеева.
Молекулы
Молекула — это мельчайшая частица вещества, обладающая свойствами этого вещества. Так, молекула сахара — сладкая, а соли — соленая.
Молекулы состоят из атомов.
Размеры молекул ничтожно малы.
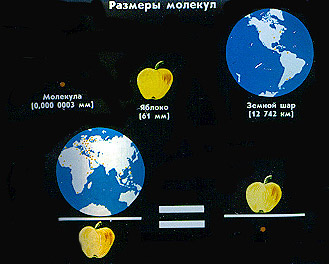
Как увидеть молекулу? — с помощью электронного микроскопа.

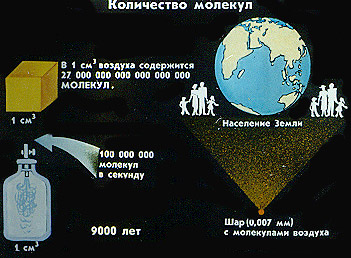
Как добыть молекулу из вещества? — механическим дроблением вещества.
Каждому веществу соответствует определеенный вид молекул. У разных веществ молекулы могут состоять из одного атома (инертные газы) или из нескольких одинаковых или различных атомов, или даже из сотен тысяч атомов (полимеры). Молекулы различных веществ могут иметь форму треугольника, пирамиды и других геометрических фигур, а также быть линейными.
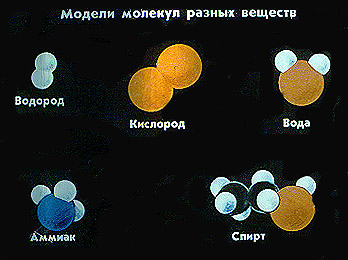
Молекулы одного и того же вещества во всех агрегатных состояниях одинаковы.

Между молекулами в веществе существуют промежутки. Доказательствами существования промежутков служат изменение объема вещества, т.е. расширение и сжатие вещества при изменении температуры, и явление диффузии. Молекулы вещества находятся в непрерывном тепловом движении.
КНИЖНАЯ ПОЛКА
С чем едят тефлон? ………. смотреть
Инопланетное чудо ………. смотреть
Что тоньше всего? ………. смотреть
Движущаяся ракета ………. смотреть
Расходящиеся кольца ………. смотреть
НЕУЖЕЛИ?
Если бы размер молекулы увеличить до размера точки в конце предложения в книге, то толщина человеческого волоса стала бы равна 40м, а человек, стоя на поверхности Земли, упирался бы головою в Луну!
Если из детского резинового шарика, надутого и наполненного водородом (массой 3г), каждую секунду выпускать по 1 миллиону молекул, то понадобится 30 миллиардов лет!
Если удалить пространство из всех атомов человеческого тела, то все, что останется, сможет пролезть через игольное ушко.
ВЕСЁЛЫЕ ЗАДАЧКИ!
— жми здесь!
ПОЧЕМУ?
1. Рука золотой статуи в древнегреческом храме, которую целовали прихожане, за десятки лет заметно похудела. Почему?
2. Почему появляются углубления в ступенях древних каменных лестниц?
3. Почему изнашиваются подметки у ботинок, и стираются до дыр локти пиджаков?
4. Чем отличается движение одной и той же молекулы в воздухе и в вакууме?
ОПРЕДЕЛЕНИЕ РАЗМЕРОВ МАЛЫХ ТЕЛ МЕТОДОМ РЯДОВ
Если вам необходимо определить размеры очень маленького тела (хотя бы макового зернышка), и осуществить это с помощью измерительных приборов (например, линейки) невозможно, следует прибегнуть к «методу рядов».

Расположите некоторое количество тел вплотную друг к другу в ряд, измерьте длину ряда и рассчитайте по формуле размер «l» одного тела.
N — количество тел в ряду
L — длина ряда
Проверьте, не поленитесь, это очень удобно!
Следующая страница
Назад в раздел «Занимательные фишки по физике для 7 класса»
Свойства и строение жидкостей
Жидкости склонны к легкому изменению своей формы с сохранением объема. В стандартных условиях они привычно принимают форму емкости, в которой находятся. Поверхность жидкости, что не соприкасается со стенками сосуда, называется свободной. Ее образование происходит вследствие воздействия силы тяжести на молекулы жидкости.
Свойства жидкостей можно объяснить малыми промежутками между их молекулами малы. Так, молекулы упакованы настолько плотным образом, что расстояние между каждыми двумя из них оказывается меньше их размеров.
Объяснить поведение жидкостей на основании характера молекулярного движения, взялся советский ученый Я. И. Френкель. Согласно его исследованию, молекула жидкости будет колебаться около положения временного равновесия, при этом происходит ее столкновение с остальными молекулами из ближнего окружения. Периодически у нее получается совершить «прыжок», чтобы, покинув своих «соседей», продолжить совершать колебания уже в кругу новых.
Замечание 1
По причине малых расстояний между молекулами жидкости, попытка уменьшения объема приводит к состоянию деформации молекул, так начинается их отталкивание друг от друга, чем можно объяснить малую сжимаемость жидкости. В то же время, ее текучесть объясняют тем фактом, что «прыжки» молекул из оседлого положения в иное осуществляются, согласно всем направлениям с равной частотой. Внешняя сила не изменяет существенно число «прыжков» за секунду, а только задает их преимущественное направление, поэтому жидкость и принимает форму сосуда, в котором пребывает.
Радиация
В процессе распада вещества или его синтеза происходит выброс элементов атома (протонов, нейтронов, электронов, фотонов), иначе можно сказать происходит излучение этих элементов. Подобное излучение называют — ионизирующее излучение или что чаще встречается радиоактивное излучение, или еще проще радиация. К ионизирующим излучениям относится так же рентгеновское и гамма излучение.
Радиоактивное излучение, сталкиваясь с материей, проникает в нее, начинает взаимодействовать с атомами и молекулами, вырывая электроны с внешних оболочек атомов, что приводит к изменению заряда атома.
Ионизация — это процесс образования положительно или отрицательно заряженных ионов или свободных электронов из нейтрально заряженных атомов или молекул.
Все элементарные частицы атома обладают огромной энергией и движутся с большими скоростями. В процессе радиоактивного (ионизирующего) излучения, излучаемые элементы сталкиваются с материей, встречающейся у нее на пути, и оказывают на нее мощное энергетическое воздействие. В этом и кроется основная опасность радиации как процесса или воздействия. Под воздействием радиации, как живая, так и не живая материя, может претерпевать значительные изменения, поглощая энергию излучения.
От того, какие элементы излучаются атомом вещества в виде радиации, зависит степень воздействия радиации на вещество.
Атомистическая гипотеза
Еще в Древней Греции философами Левкиппом и Демокритом было введено понятие атомов – неких фундаментальных мельчайших блоков, слагающих материю. В эпоху паровых двигателей и становления термодинамики к этой концепции вернулись. Дальтон, Ломоносов, Лавуазье и прочие великие умы внесли вклад в формирование атомистической гипотезы, которая, тем не менее, так и не объяснила, какова структура вещества.
Считалось, что атомы – это некие неделимые частицы (корпускулы), находящиеся в постоянном движении, и из них слагалась вся материя. Такой подход позволил решить назревшие проблемы и создать новые технологии, но не более.
Молекулярная теория воды
Существует ряд определенных гипотез, объясняющих строение льда, пара, воды. Все они в какой-то степени опираются на молекулярно-кинетическую теорию строения вещества, чьи основы заложил М. Ломоносов.
 Рисунок 2. Масса и размеры молекул. Автор24 — интернет-биржа студенческих работ
Рисунок 2. Масса и размеры молекул. Автор24 — интернет-биржа студенческих работ
Данная теория исходит из принципов классической механики, что рассматривает молекулы (атомы) в формате шариков правильной формы, электрически нейтральных, идеально упругих. Такие молекулы склонны подвергаться исключительно механическим соударениям и не испытывать каких-либо электрических сил взаимодействия.
Водяной пар, согласно положениям молекулярно-кинетической теории, представляет собрание молекул, расстояние между ними многократно превышает размеры самих молекул. Молекулы газа, пребывающие в непрерывно-хаотическом движении, пробегают путь между стенками сосудов, где заключен газ и при этом происходит их столкновение между собой на данном пути.
При приближении температуры газа к температуре кипения (100°C) наступает уменьшение скорости молекул, и при соударении силы притяжения между ними возникает больше сил упругих отталкиваний в момент удара. По этой причине газ способен конденсироваться в жидкость.
Замечание 2
Жидкость, в отличие от газа, является совокупностью близкорасположенных между собой молекул. Это расположение настолько близкое, что между ними начинается проявление сил взаимного притяжения. Это не позволяет молекулам жидкости разлетаться в разные стороны, подобно молекулам газа, а только колебаться около собственного равновесного положения.
Наряду с тем, из-за недостаточной плотности строения жидкости, в ней присутствуют свободные места, вследствие чего (исходя из теории Френкеля), обладающие большей энергией молекулы начинают вырываться из своего привычного окружения и скачкообразно перемещаться в соседнее отверстие на расстоянии, равном размерам самих молекул.
Таким образом, молекулы в жидкости относительно редко перемещаются в иные места, большую часть времени они пребывают в «оседлом» состоянии, подвергаясь только колебаниям. При температуре в 100°C (при нормальном атмосферном давлении) вода начнет распадаться на отдельные молекулы, скорость которых уже не способна к преодолению взаимного молекулярного притяжения, поэтому вода становится паром.
В случае охлаждения жидкости можно наблюдать обратный процесс. Начинается уменьшение скоростей колебательного движения молекул, становится более прочной структура жидкости, а сама она переходит в состояние льда (кристаллическое).
Из чего все состоит. Молекулы
Сейчас тела рассматривают при помощи очень мощных электронных микроскопов. Через них видно, что вещество представлено множеством мельчайших подвижных «кирпичиков». У разных веществ эти «кирпичики» различны. Их называют молекулами. А если представить, что глаза – это «глаза-микроскопы», то мысленно можно увидеть эти маленькие частички.
Молекулы, оказывается, состоят из атомов, а они еще более мелкие частицы. Например, атомы кислорода и водорода, объединившись, образуют знаменитую молекулу воды. Существует шутливая фраза: «Сапоги мои того – пропускают Н2О». Н2О – химическая формула молекулы вода. Н – обозначение водорода, О – кислорода. Индекс 2 в данному случае обозначает число атомов водорода в составе молекулы воды. Молекулы газов водорода и кислорода уже новые. В них по два атома водорода и кислорода (Н2 и О2).
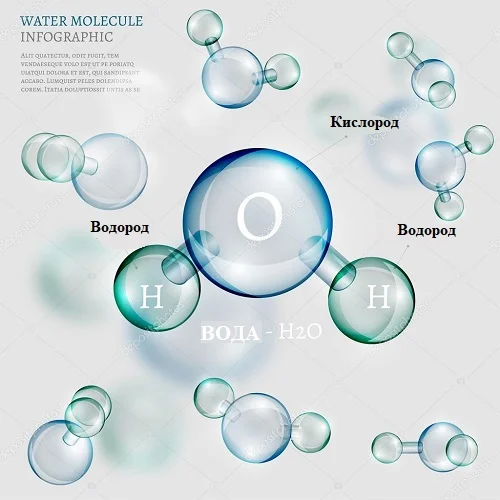
Существуют вещества, состоящие только из атомов. Это металлы и инертные газы (например, неон в рекламной иллюминации). Различные комбинации атомов порождают новые вещества, существующие в природе.
Люди очень давно предполагали, что вещества составлены из молекул и атомов. Еще в пятом веке до нашей эры ученый Древней Греции Демокрит высказал такую гипотезу. В России учение о молекулярном строении вещества развил М.В. Ломоносов в восемнадцатом веке.
Как же оценить размеры загадочных маленьких частиц?
Следуя правилу измерения, их нужно с чем-то сравнить. Интересен такой мысленный эксперимент: семиклассник и молекула. Если молекулу увеличить в несколько раз так, чтобы она стала размером с семиклассника, но и его увеличить во столько же раз, то семиклассник может достать до Солнца. Наука, конечно, не пользуется такими сравнениями. Современные приборы — микроскопы позволяют найти размеры атомов и молекул довольно точно. Существует возможность подсчитать и количество маленьких частиц в любом теле.
Легко догадаться, что число молекул вещества огромно. И опять интересное сравнение: если бы людей на планете Земля было столько, сколько молекул в одном кубическом сантиметре воздуха, то на одном квадратном километре Земли могли бы уместиться пять тысяч человек.
Итак, вещество состоит из молекул, а молекулы из атомов;
- разные вещества по структуре имеют разные молекулы (комбинации атомов);
- молекулы микроскопически малы, а в теле их огромное количество.
Опыты
Какие опыты подтверждают, что вещества состоят из мельчайших частиц? Сейчас мы и их и рассмотрим.
Опыт с нагреванием и охлаждением твердого тела
Если мы приложим к определенному телу некоторое усилие, мы можем уменьшить объем этого тела. Например, теннисного мячика, воздушного шарика, кусочка воска. Но объем тела также изменяется при его нагревании или охлаждении.
Давайте проверим это утверждение на простом опыте. Возьмем медный шарик, который в обычном состоянии спокойно проходит через кольцо (рисунок 2, а), закрепленное на штативе.
А теперь нагреем шарик. Мы увидим, что через кольцо он уже не проходит (рисунок 2, б). Шарик увеличился в размерах при нагревании.
Рисунок 2. Опыт с нагреванием твердого тела
Когда же он остынет, то снова начнет проходить через кольцо. Получается, что при нагревании твердое тело увеличивается в объеме, а при охлаждении — уменьшается.
{"questions":,"answer":}}}]}
Опыт с нагреванием жидкости
Теперь давайте проведем похожий опыт с жидкостью. Посмотрим, как она будет вести себя при нагревании.
Наполним колбу водой. Плотно закроем ее пробкой, через которую будет проходить стеклянная трубка. Отметим уровень жидкости в трубке (рисунок 3, а). Начнем нагревать нашу жидкость, и увидим, что уровень воды в трубке начнет подниматься (рисунок 3, б).
Рисунок 3. Опыт с нагреванием жидкости в колбе
Как меняется объем тела при изменении расстояния между частицами?Так как все вещества состоят из отдельных частиц, можно предположить, что объем тела увеличивается, когда увеличивается расстояние между этими частичками. И наоборот, когда расстояние между частицами уменьшается, объем тела становится меньше.
После этих опытов мы можем сделать вывод.
{"questions":,"answer":}}}]}
Опыт с окрашиванием воды
Так почему же мы не видим этих частиц, из которых состоят вещества? Современная наука доказала, что размер частиц невероятно мал, и мы просто не можем увидеть их невооруженным взглядом.
Но мы можем доказать факт существования этих частиц на следующем простейшем опыте (рисунок 4). Возьмем колбу с водой и растворим в ней каплю фиолетовой краски. Что произойдет? Вода окрасится в фиолетовый цвет (колба №1).
Рисунок 4. Опыт с окрашиванием воды в разных колбах
Далее отольем немного воды из колбы №1 в пустую колбу №2 и дольем в нее чистую воду. Теперь вода в колбе №2 будет окрашена не так интенсивно, как в колбе №1.
Ту же самую операцию проделаем с колбой №3, но окрашенную воду будем доливать из колбы №2. Таким образом, мы получим в колбе №3 самый бледный оттенок окрашенной воды.
Как же этот опыт подтверждает гипотезу о том, что все вещества состоят из частиц? Поскольку в колбу №1 попала всего лишь 1 капля зелёной краски, а окрасилась вода и в остальных колбах.
Можно предположить, что эта капля в свою очередь состояла из огромного множества мелких частиц, которые и оказались во всех трех колбах.
Именно этот опыт показывает, что частицы вещества очень малы.
{"questions":,"answer":}}}]}
Строение вещества
Мельчайшей частицей вещества, которая определяет все свойства данного вещества, является молекула. Молекула состоит из атомов. Число атомов и их распределение в молекуле является различным. В природе существует немногим более сотни атомов различного вида. Элементы обобщены и расположены в периодической таблице химических элементов, им даны наименования, например, водород, азот, углерод.
Движение частиц вещества называют тепловым движением.
Броуновское движение — беспорядочное движение микроскопических видимых, плавающих в жидкости или газе частиц твёрдого вещества, вызываемое тепловым движением частиц жидкости или газа.
Взаимное проникновение частиц одного вещества в другое, обусловленное движением молекул, называют диффузией (от латинского «диффузио» — распространение, растекание).
Состояние вещества.
Вещества в природе встречаются в трёх состояниях:
- твёрдом
- жидком
- газообразном
Твёрдые тела сохраняют объём и форму. Жидкости сохраняют объём, но легко меняют свою форму. Газы не имеют постоянного объёма и собственной формы. Редко встречающимся состоянием вещества является плазма, которая сходна с газом и излучает свет. Плазму часто называют четвёртым агрегатным состоянием вещества.
Молекулы одного и того же вещества в различных состояниях не отличаются друг от друга. Различные свойства вещества во всех состояниях определяются тем, что его молекулы расположены иначе и движутся по-разному.
Каждому твёрдому телу характерна твёрдость. Твёрдость — способность тела сопротивляться воздействию другого тела. Твёрдость вещества выясняют, царапая его каким-либо другим веществом.
Существуют различные шкалы твёрдости. Одна из них составлена в 1811 году немецким минералогом Фридрихом Моосом. Она состоит из 10 уровней, самым мягким веществом в ней является тальк, а самым твёрдым — алмаз. Алмаз в 58 раз твёрже стоящего на втором месте по твёрдости минерала корунда, из которого изготавливают рубины и сапфиры.
Свойством тел, изготовленных из твёрдого вещества, является их деформация. Деформация — изменение формы или размера тела под воздействием другого тела.
Эластичностью называют возможность тела после деформации возвращать себе первоначальную форму. Пластилин является пластичным, ему легко придать любую форму, которая сохраняется.
Прочность — способность вещества сопротивляться разрушению. У каждого материала имеется свой предел прочности. Стекло нельзя гнуть, т.к. оно хрупкое. Очень прочными являются металлы.
Кристаллы — это твёрдые тела, в которых атомы расположены закономерно, упорядоченно, образуя кристаллическую решётку. Это лёд, соль, металлы, минералы и т.д.
Аморфные тела — тела, не имеющие строгой кристаллической решётки, бесформенные тела. («аморфный» происходит от греч. «аморфос» — бесформенный)
В отличие от кристаллов, стабильно-аморфные вещества не затвердевают с образованием кристаллических граней.
Структуры жидкостей и аморфных тел имеют много общего. По этой причине принято считать аморфные тела очень густыми, вязкими, застывшими жидкостями. Аморфные вещества могут находиться либо в стеклообразном состоянии при низких температурах, либо в состоянии расплава при высоких температурах. Аморфные тела обладают текучестью, хотя и значительно меньшей, чем жидкости. При повышении температуры текучесть аморфных тел увеличивается. Благодаря этому из капли нагретого стекла можно выдуть стеклянный сосуд.
Это конспект по теме «Строение вещества». Ваши дальнейшие действия:
- Пройти тест по теме Строение вещества
- Перейти к следующему конспекту: Масса и плотность.
- Вернуться к списку конспектов по Физике.
Строение вещества
Все что мы видим вокруг, что нас окружает, состоит из крошечных кирпичиков — молекул, которые в свою очередь состоят из атомов. Атомы состоят из еще более мелких частиц — нейтронов, протонов, электронов. Одна молекула может содержать несколько различных атомов, количество и вид которых определяет химические и физические свойства вещества. Например, одна молекула воды состоит из двух атомов водорода и одного атома кислорода.
Структура любого атома похожа на миниатюрную модель солнечной системы, у которой в центре расположено ядро, состоящее из нейтронов и протонов, а вокруг ядра вращаются электроны. Каждый элемент атома имеет свой заряд: электрон — отрицательный; протон — положительный; нейтрон — нейтрален. В нормальном состоянии атом имеет нейтральный заряд, так как количество электронов и протонов всегда одинаковое.
От количества протонов в ядре атома зависит к какому химическому элементу относится сам атом. У одного и того же химического элемента в ядре атома может содержаться различное количество нейтронов. Например, атом водорода в своем ядре может содержать один или два протона, либо вообще не содержать протонов. При этом все три вида вещества будут относится к одному химическому элементу — водороду, но будут иметь разные физические свойства. Подобные элементы называются изотопами элемента. Группа изотопов одного элемента называется — нуклидами.
Значительная часть изотопов из-за своей сложной структуры и большого количества элементов в ядре атома, имеют не стабильную структуру и как следствие непродолжительное время существования. Если в ядре атома количество протонов и нейтронов сильно различается, то такой элемент является нестабильным. В результате одни элементы распадаются, образуя более простые элементы, а те в свою очередь так же могут распадаться на еще более простые и стабильные элементы. Данный процесс называется радиоактивным распадом вещества, а время, за которое часть вещества распадается, называется периодом полураспада вещества. Одни элементы могут оставаться стабильными миллиарды лет, другие могут существовать лишь тысячные доли секунды. Процесс распада в природе происходит по определённым цепочкам, от одного вещества к другому на протяжении всего существования материи.
Существует и обратный процесс, кода из более простых веществ, образуются более сложные вещества — данный процесс называется синтезом. Подобные процессы происходят в звездах и других небесных телах, в которых протекают активные термоядерные реакции. Например, в нашем солнце один из основных процессов, это слияние молекул водорода и образование из них молекул гелия.



























